题目内容
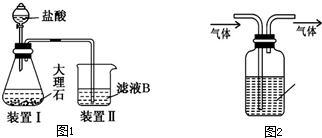
4.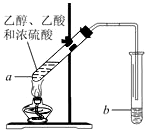 如图,在左试管中先加入3mL的乙醇,并在摇动下缓缓加入2mL浓硫酸,再加入2mL乙酸,充分摇匀.在右试管中加入5mL饱和Na2CO3溶液.按图连接好装置,用酒精灯缓慢加热.
如图,在左试管中先加入3mL的乙醇,并在摇动下缓缓加入2mL浓硫酸,再加入2mL乙酸,充分摇匀.在右试管中加入5mL饱和Na2CO3溶液.按图连接好装置,用酒精灯缓慢加热.(1)写出左试管中主要反应的方程式CH3COOH+CH3CH2OH
 CH3COOCH2CH3+H2O;
CH3COOCH2CH3+H2O;(2)加入浓硫酸的作用:催化剂;吸水剂;
(3)饱和Na2CO3的作用是:除去乙酸;吸收乙醇;降低乙酸乙酯的溶解度便于分层.
(4)反应开始时用酒精灯对左试管小火加热的原因是:加快反应速率;
同时防止反应物未来得及反应而挥发损失;(已知乙酸乙酯的沸点为77℃;乙醇的沸点为78.5℃;乙酸的沸点为117.9℃)
(5)分离右试管中所得乙酸乙酯和Na2CO3溶液的操作为(只填名称)分液.
分析 (1)乙酸与乙醇在浓硫酸作用下发生酯化反应生成乙酸乙酯和水;
(2)浓硫酸加快反应速率,且吸收水;
(3)饱和碳酸钠吸收乙酸、乙醇,降低乙酸乙酯的溶解度;
(4)对左试管小火加热,由沸点可知,减少反应物挥发,同时加快反应速率;
(5)乙酸乙酯和Na2CO3溶液分层.
解答 解:(1)乙酸与乙醇在浓硫酸作用下发生酯化反应生成乙酸乙酯和水,则反应为CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O,
CH3COOCH2CH3+H2O,
故答案为:CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O;
CH3COOCH2CH3+H2O;
(2)该实验中加入浓硫酸的作用为催化剂、吸水剂,故答案为:催化剂;吸水剂;
(3)饱和Na2CO3的作用是除去乙酸、吸收乙醇、降低乙酸乙酯的溶解度便于分层,
故答案为:除去乙酸;吸收乙醇;降低乙酸乙酯的溶解度便于分层;
(4)对左试管小火加热,由沸点可知,反应开始时用酒精灯对左试管小火加热的原因是加快反应速率、同时防止反应物未来得及反应而挥发损失,
故答案为:加快反应速率;同时防止反应物未来得及反应而挥发损失;
(5)乙酸乙酯和Na2CO3溶液分层,则分离操作为分液,故答案为:分液.
点评 本题考查有机物的制备实验,为高频考点,把握制备实验原理、物质的性质、混合物分离、反应速率影响因素等为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.已知25℃时有关弱酸的电离平衡常数:弱酸化学式 CH3COOH HCN H2CO3电离平衡常数(25℃)1.8×l0-54.9×l0-10K1=4.3×l0-7 K2=5.6×l0-11则下列有关说法正确的是( )
| A. | 将a molL-1 HCN溶液与a molL-1 NaOH溶液等体积混合,混合液中:c(OH-)>c(H+),c(Na+)>c(CN-) | |
| B. | 等物质的量浓度的各溶液pH关系为:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) | |
| C. | 冰醋酸中逐滴加水,溶液的导电性、醋酸的电离程度、pH均先增大后减小 | |
| D. | NaHCO3和Na2CO3混合液中,一定有c(Na+)+c(H+)═c(OH-)+c(HCO3-)+c(CO32-) |
19.下列各选项从左至右按互为同位素、互为同系物、互为同分异构体、互为同素异形体、是同种物质顺序排列的是( )
①C60、C70、金刚石、石墨
②C2H5OH、CH3OCH3
③${\;}_{6}^{12}$C、${\;}_{6}^{13}$C、${\;}_{6}^{14}$
④HOCH2COOH、HOCH2CH2COOH、HOCH2CH2CH2COOH
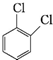
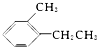
⑤ 、
、
①C60、C70、金刚石、石墨
②C2H5OH、CH3OCH3
③${\;}_{6}^{12}$C、${\;}_{6}^{13}$C、${\;}_{6}^{14}$
④HOCH2COOH、HOCH2CH2COOH、HOCH2CH2CH2COOH
⑤
 、
、
| A. | ①②③⑤④ | B. | ③⑤④①② | C. | ④②①⑤③ | D. | ③④②①⑤ |
9.NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下,11.2 L的苯所含的分子个数为0.5NA | |
| B. | 28 g乙烯所含共用电子对数目为4NA | |
| C. | 标准状况下,11.2 L二氯甲烷所含原子个数为2.5NA | |
| D. | 现有乙烯、丙烯、丁烯的混合气体共14 g,其原子个数为3NA |
14.下列有机物的命名正确的是( )
| A. | 二溴乙烷: | B. | 3-乙基-1-丁烯: | ||
| C. | 2-甲基-2,4-己二烯: | D. | 2,2,3-三甲基戊烷: |
 .
.
 ②
②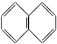 ③
③ ④TNT
④TNT