题目内容
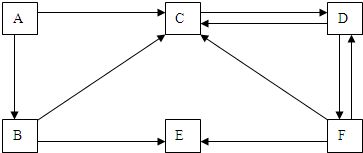
A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(副产物已略去)
A
B
C
试回答:
(1)若X是强氧化剂的单质,则A可能是
a.Nab.Mgc.Ald.Ce.Si
(2)若X为金属单质,向C的水溶液中滴加AgNO3溶液产生不溶于稀硝酸的白色沉淀,则①B的溶液用于刻制印刷电路板中铜的“腐蚀液”时发生反应的化学方程式为 ;②贮存C溶液中应加入少量X目的是 (用离子方程式表示);③检验C中金属阳离子的试剂为 .(若为多种,按使用顺序填写)
(3)若A、B、C为含有同一金属元素的化合物,X为强电解质,则反应②的离子方程式为 .
(4)若A、B、C为含有同一金属元素的化合物,X为非电解质,且A溶液与C溶液反应生成B溶液,则当向100ml 2mol/L的A溶液中通入标准状况下3.36L的X时,写出该反应的离子方程式 .
A
| +X一定条件 |
| 反应① |
| +X一定条件 |
| 反应② |
试回答:
(1)若X是强氧化剂的单质,则A可能是
a.Nab.Mgc.Ald.Ce.Si
(2)若X为金属单质,向C的水溶液中滴加AgNO3溶液产生不溶于稀硝酸的白色沉淀,则①B的溶液用于刻制印刷电路板中铜的“腐蚀液”时发生反应的化学方程式为
(3)若A、B、C为含有同一金属元素的化合物,X为强电解质,则反应②的离子方程式为
(4)若A、B、C为含有同一金属元素的化合物,X为非电解质,且A溶液与C溶液反应生成B溶液,则当向100ml 2mol/L的A溶液中通入标准状况下3.36L的X时,写出该反应的离子方程式
考点:无机物的推断
专题:
分析:(1)X是强氧化性单质,能发生连续氧化,则A为S、N2、C、钠等;
(2)向C的溶液中滴加AgNO3溶液,产生不溶于稀硝酸的白色沉淀,则A、B、C含有Cl元素,X是金属单质,结合反应特点可知X应为变价金属,应为Fe,则A应为Cl2,B为FeCl3,C为FeCl2;
(3)若A、B、C为含有金属元素的无机化合物,X为强酸或强碱,则B应为Al(OH)3,若X是强碱,则A为铝盐,C为偏铝酸盐,若X为强酸,则A为偏铝酸盐,C为铝盐;
(4)若A、B、C为含有同一金属元素的化合物,X为非电解质,且A溶液与C溶液反应生成B溶液,A可以为氢氧化钠,则X为二氧化碳,B为碳酸钠,C为碳酸氢钠;
(2)向C的溶液中滴加AgNO3溶液,产生不溶于稀硝酸的白色沉淀,则A、B、C含有Cl元素,X是金属单质,结合反应特点可知X应为变价金属,应为Fe,则A应为Cl2,B为FeCl3,C为FeCl2;
(3)若A、B、C为含有金属元素的无机化合物,X为强酸或强碱,则B应为Al(OH)3,若X是强碱,则A为铝盐,C为偏铝酸盐,若X为强酸,则A为偏铝酸盐,C为铝盐;
(4)若A、B、C为含有同一金属元素的化合物,X为非电解质,且A溶液与C溶液反应生成B溶液,A可以为氢氧化钠,则X为二氧化碳,B为碳酸钠,C为碳酸氢钠;
解答:
解:(1)X是强氧化性单质,能发生连续氧化,则A为S、N2、C、钠等,而Mg、Al、Si不能发生连续氧化,则A不可能为Mg、Al、Si,故答案为:ad;
(2)向C的溶液中滴加AgNO3溶液,产生不溶于稀硝酸的白色沉淀,则A、B、C含有Cl元素,X是金属单质,结合反应特点可知X应为变价金属,应为Fe,则A应为Cl2,B为FeCl3,C为FeCl2,①B的溶液用于刻制印刷电路板中铜的“腐蚀液”时发生反应的化学方程式为Cu+2FeCl3=CuCl2+2FeCl2;②贮存C溶液中应加入少量X目的是防止Fe2+被氧化,离子方程式为2Fe3++Fe═3Fe2+;③检验C中金属阳离子为Fe2+,可以先加KSCN试剂,溶液元素明显变化,再加双氧水或氯水,溶液出现血红色,则说明原溶液中有Fe2+,
故答案为:Cu+2FeCl3=CuCl2+2FeCl2;2Fe3++Fe═3Fe2+;KSCN、双氧水或氯水;
(3)若A、B、C为含有同一金属元素的化合物,X为强电解质,即X可以为强酸或强碱或盐,若X是强碱,则A可以为铝盐,B应为Al(OH)3,C为偏铝酸盐,若X为强酸,则A可以为偏铝酸盐,则B应为Al(OH)3,C为铝盐,A也可以为Na2CO3,则B为NaHCO3,C为CO2,所以反应②的离子方程式可能为:Al3Al(OH)3+OH-=AlO2-+2H2O或Al(OH)3+3H+=Al3++3H2O或,HCO3-+H+=CO2+H2O,
故答案为:Al(OH)3+OH-=AlO2-+2H2O或Al(OH)3+3H+=Al3++3H2O或HCO3-+H+=CO2+H2O;
(4)若A、B、C为含有同一金属元素的化合物,X为非电解质,且A溶液与C溶液反应生成B溶液,A可以为氢氧化钠,则X为二氧化碳,B为碳酸钠,C为碳酸氢钠,则当向100ml 2mol/L即0.2mol的NaOH溶液中通入标准状况下3.36L即0.15mol的CO2时,NaOH和CO2的物质的量之比为0.2:0.15=4:3,该反应的离子方程式为4OH-+3CO2=2HCO3-+CO32-+H2O,
故答案为:4OH-+3CO2=2HCO3-+CO32-+H2O;
(2)向C的溶液中滴加AgNO3溶液,产生不溶于稀硝酸的白色沉淀,则A、B、C含有Cl元素,X是金属单质,结合反应特点可知X应为变价金属,应为Fe,则A应为Cl2,B为FeCl3,C为FeCl2,①B的溶液用于刻制印刷电路板中铜的“腐蚀液”时发生反应的化学方程式为Cu+2FeCl3=CuCl2+2FeCl2;②贮存C溶液中应加入少量X目的是防止Fe2+被氧化,离子方程式为2Fe3++Fe═3Fe2+;③检验C中金属阳离子为Fe2+,可以先加KSCN试剂,溶液元素明显变化,再加双氧水或氯水,溶液出现血红色,则说明原溶液中有Fe2+,
故答案为:Cu+2FeCl3=CuCl2+2FeCl2;2Fe3++Fe═3Fe2+;KSCN、双氧水或氯水;
(3)若A、B、C为含有同一金属元素的化合物,X为强电解质,即X可以为强酸或强碱或盐,若X是强碱,则A可以为铝盐,B应为Al(OH)3,C为偏铝酸盐,若X为强酸,则A可以为偏铝酸盐,则B应为Al(OH)3,C为铝盐,A也可以为Na2CO3,则B为NaHCO3,C为CO2,所以反应②的离子方程式可能为:Al3Al(OH)3+OH-=AlO2-+2H2O或Al(OH)3+3H+=Al3++3H2O或,HCO3-+H+=CO2+H2O,
故答案为:Al(OH)3+OH-=AlO2-+2H2O或Al(OH)3+3H+=Al3++3H2O或HCO3-+H+=CO2+H2O;
(4)若A、B、C为含有同一金属元素的化合物,X为非电解质,且A溶液与C溶液反应生成B溶液,A可以为氢氧化钠,则X为二氧化碳,B为碳酸钠,C为碳酸氢钠,则当向100ml 2mol/L即0.2mol的NaOH溶液中通入标准状况下3.36L即0.15mol的CO2时,NaOH和CO2的物质的量之比为0.2:0.15=4:3,该反应的离子方程式为4OH-+3CO2=2HCO3-+CO32-+H2O,
故答案为:4OH-+3CO2=2HCO3-+CO32-+H2O;
点评:本题考查无机物的推断,侧重于考查学生对元素化合物知识的综合理解和运用,注意把握A连续与X反应的特点,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
能影响水的电离平衡,并使溶液中的c(H+)>c(OH-)的操作是( )
| A、向水中投入一小块金属钠 |
| B、将水加热煮沸 |
| C、向水中加入硝酸铵晶体 |
| D、向水中加食盐晶体 |
某种合成树脂的结构可表示为:
?
则生成该树脂的单体的种类和化学反应所属类型正确的是( )
?

则生成该树脂的单体的种类和化学反应所属类型正确的是( )
| A、1种 加聚反应 |
| B、2种 缩聚反应 |
| C、3种 加聚反应 |
| D、3种 缩聚反应 |
人体细胞组织中含量最多的营养物质是( )
| A、蛋白质 | B、糖类 | C、脂肪 | D、水 |
维生素C也称抗坏血酸.人体对维生素C的主要摄入途径是( )
| A、米饭 | B、新鲜水果和蔬菜 |
| C、肉类 | D、牛奶 |
研究人员研制出一种锂水电池,做军事上重要的能源.该电池以金属锂和钢板为电极材料,以LiOH为电解质,使用时加入水即可放电.关于该电池的下列说法不正确的是( )
| A、水既是氧化剂又是溶剂 |
| B、总反应为:2Li+2H2O=2LiOH+H2↑ |
| C、放电时正极上有氢气生成 |
| D、放电时OH-向正极移动 |