题目内容
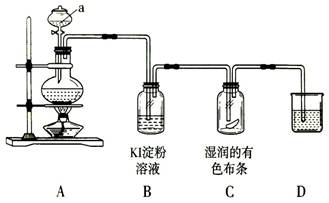
14.在实验室中用MnO2和浓盐酸反应制备纯净干燥的氯气时,如图是某学生设计的实验装置图.
①请指出下述装置中的4个错误
Ⅰ.使用长颈漏斗添加盐酸;
Ⅱ.使用稀盐酸;
Ⅲ.缺少酒精灯;
Ⅳ.缺少尾气处理装置
②实验室制取氯气的化学方程式:MnO2+4HCl(浓)$\frac{\underline{\;加热\;}}{\;}$MnCl2+Cl2↑+2H2O.
③因浓HCl有挥发性,制的Cl2中常混有杂,常用饱和食盐水除HCl,用浓硫酸除水蒸气
④检验Cl2用湿润的KI淀粉试纸,有关反应的化学方程式为2KI+Cl2═2KCl+I2.因Cl2有毒污染空气,用NaOH溶液吸收多余的氯气,反应的化学方程式为2NaOH+Cl2═NaCl+NaClO+H2O.
分析 ①本题的实验目的是制得纯净、干燥的氯气,用MnO2和浓盐酸共热制得的氯气中,有挥发出来的HCl气体和水蒸气,这是两种要除掉的杂质.用饱和食盐水进行水洗是为了除去HCl气体,用浓硫酸洗气瓶是为了除掉水蒸气,为达到目的,应先除HCl,后除水蒸气,且洗气装置应长管进、短管出,另外,本反应的条件是加热,且给烧瓶加热时应垫上石棉网,据此解答.
②实验室是用MnO2和浓盐酸在加热条件下制备来氯气;
③制备的氯气中有挥发出来的HCl气体和水蒸气,先用饱和食盐水除去HCl气体,再用浓硫酸吸收水蒸气,
④氯气本身具有氧化性,KI具有还原行,因此氯气能与KI反应生成碘单质,可以检验氯气;氯气有毒不能直接排放到空气中,可以用氢氧化钠溶液吸收.
解答 解:①二氧化锰和浓盐酸制取氯气时应该用浓盐酸而不是稀盐酸,滴加浓盐酸时应用分液漏斗需,加热药品时圆底烧瓶不能直接加热,氯气有毒应该有尾气处理;
故答案为:使用长颈漏斗添加盐酸;使用稀盐酸;缺少酒精灯;缺少尾气处理装置;
②实验室是用MnO2和浓盐酸在加热条件下制备来氯气;故答案为:MnO2+4HCl(浓)$\frac{\underline{\;加热\;}}{\;}$ MnCl2+Cl2↑+2H2O
③因浓HCl有挥发性,制的Cl2中常混有HCl与水蒸气,常用饱和食盐水除去HCl,用浓硫酸除去水蒸气,其顺序是先通过饱和食盐水,再通过浓硫酸;
故答案为:HCl;水蒸气;
④用湿润的KI淀粉试纸检验,现象是试纸变蓝,有关反应的化学方程式为:2KI+Cl2═2KCl+I2,Cl2有毒污染空气,且是酸性气体,因此用NaOH溶液吸收多余的氯气,故答案为:2KI+Cl2═2KCl+I2;NaOH溶液;2NaOH+Cl2═NaCl+NaClO+H2O.
点评 本题为考查氯气的实验室制法,熟悉实验室制取氯气的反应原理和实验过程是解题关键,注意除杂的顺序,题目难度不大

 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案| A. | 2H2(g)+O2(g)═2H2O(1)△H=-571.6kJ/mol | B. | 2H2(g)+O2(g)═2H2O(1)△H=+571.6 kJ/mol | ||
| C. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-285.8 kJ/mol | D. | H2(g)+$\frac{1}{2}$O2(g)═H2O(1)△H=-285.8kJ/mol |
| A. |  | B. |  | C. |  | D. |  |
| 1.0 MPa | 2.0 MPa | 3.0 MPa | |
| 810℃ | 54.0% | a | b |
| 915℃ | c | 75.0% | d |
| 1000℃ | e | f | 83.0% |
上述①~④中正确的有( )
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
C(石墨,s)+O2(g)═CO2(g)△H=-393.5kJ•mol-1
C(金刚石,s)+O2(g)═CO2(g)△H=-395.4kJ•mol-1
据此推理所得到的下列结论中,正确的是( )
| A. | 金刚石燃烧比石墨燃烧放出的热量少 | |
| B. | 等质量是石墨燃烧放热多 | |
| C. | 石墨的能量比金刚石的能量高 | |
| D. | 由石墨制备金刚石一定是吸热反应 |
| A. | 13g锌与一定量浓硫酸恰好完全反应,生成气体的分子数为0.2NA | |
| B. | 71g氯气通入足量的水中,反应中转移的电子总数为NA | |
| C. | 由D和18O所组成的水11g,所含的中子数为4NA | |
| D. | 1molBrCl与H2O完全反应生成氯化氢和次溴酸,转移的电子数为NA |
| A. | 常温下pH=7的溶液中:Fe3+、Mg2+、SO42-、Cl-能大最共存 | |
| B. | 在含有0.1mol/L Fe3+的溶液中:SCN-、Cl-、K+不能大最共存 | |
| C. | 在含有HCO3-、SO32-、S2-、CH3COO-四种阴离子的溶液中加入足量的Na2O2固体后,CH3COO-变化最小 | |
| D. | NaHSO4溶液与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
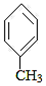 +CO$→_{△}^{AlCl_{3},HCl}$
+CO$→_{△}^{AlCl_{3},HCl}$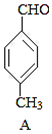 $→_{OH-,△}^{CH_{3}CHO}$B$→_{②H+}^{①C}$
$→_{OH-,△}^{CH_{3}CHO}$B$→_{②H+}^{①C}$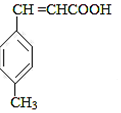 $→_{浓硫酸,△}^{CH_{3}OH}$E
$→_{浓硫酸,△}^{CH_{3}OH}$E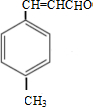 ,生成E的反应类型为酯化反应或取代反应
,生成E的反应类型为酯化反应或取代反应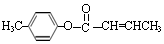 是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为
是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为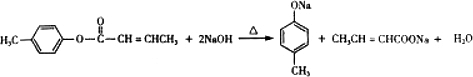 .
.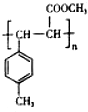 .
.