题目内容
15.氢有三种同位素:${\;}_{1}^{1}$H、${\;}_{1}^{2}$H和${\;}_{1}^{3}$H,它们之间存在差异的是( )| A. | 中子数 | B. | 电子数 | C. | 原子序数 | D. | 质子数 |
分析 同位素具有相同的质子数,不同中子数,其质量数不同,以此来解答.
解答 解:${\;}_{1}^{1}$H、${\;}_{1}^{2}$H和${\;}_{1}^{3}$H为氢元素的同位素,具有相同的质子数,不同中子数,其质量数也不同.
故选A.
点评 本题考查同位素,侧重概念的理解,把握“同”为质子数相同、化学性质几乎相同即可解答,题目难度不大.

练习册系列答案
相关题目
6.下列化学用语或模型表示正确的是( )
| A. | 氚原子符号:H | B. | H2O2分子结构式:H-O-O-H | ||
| C. | Mg2+结构示意图: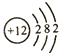 | D. | HF的形成过程 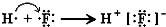 |
3.下列叙述中正确的是( )
| A. | NH3、CO、CO2都是极性分子 | |
| B. | CH4、CCl4都是含有极性键的极性分子 | |
| C. | 因为非羟基氧原子数目逐渐减少,所以酸性HClO4>H2SO4>H3PO4>HClO | |
| D. | CS2、H2O、C2H2都是直线形分子 |
20.下列物质中,属于电解质的有( )
| A. | 乙酸 | B. | 乙醇 | C. | 油脂 | D. | 氯化钠 |
7.W、X、Y、Z是原子序数依次增大的四种短周期元素,分属于连续的四个主族,电子层数之和为10,四种原子中X原子的半径最大.下列说法正确的是( )
| A. | 四种元素中有两种元素在第二周期 | |
| B. | W所在主族的元素的原子次外层电子数不可能为18 | |
| C. | X、Y、Z的最高价氧化物对应的水化物之间能两两反应 | |
| D. | 工业上获得X、Y单质的方法主要是电解其熔融的氯化物 |
4.由沸点数据:甲烷-146℃,乙烷-89℃,丁烷-0.5℃,戊烷36℃,可以判断丙烷的沸点可能是( )
| A. | 高于-0.5℃ | B. | 约是+30℃ | C. | 约是-40℃ | D. | 低于-89℃ |
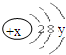 试回答:
试回答: .
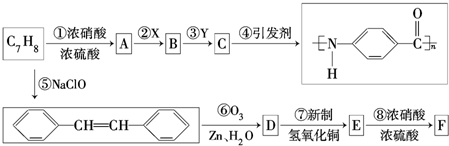
.
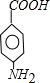 .
.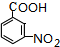 .
.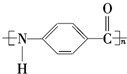 +n H2O、
+n H2O、 +2Cu(OH)2$\stackrel{△}{→}$Cu2O↓+2H2O+
+2Cu(OH)2$\stackrel{△}{→}$Cu2O↓+2H2O+ 、
、