题目内容
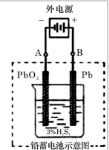
微型钮扣电池在现代生活中有广泛应用.有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH,电极反应为:Zn+2OH--2e-═ZnO+H2O Ag2O+H2O+2e-═2Ag+2OH-总反应为Ag2O+Zn═2Ag+ZnO.根据上述反应式,判断下列叙述中,正确的是( )
| A、在使用过程中,电池负极区溶液pH增大 |
| B、在使用过程中,电流由Ag2O极经外电路流向Zn极 |
| C、在使用过程中,Zn电极发生还原反应,Ag2O电极发生氧化反应 |
| D、外电路中每通过0.2mol电子,正极的质量理论上减小33.2g |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:银锌电池的电极分别是Ag2O和Zn,电解质溶液为KOH,电极反应为:Zn+2OH--2e=ZnO+H2O;Ag2O+H2O+2e=2Ag+2OH-,则Zn为负极,发生氧化反应,Ag2O为正极,发生还原反应,电子由负极流向正极,以此来解答.
解答:
解:A.负极发生Zn+2OH--2e=ZnO+H2O,c(OH-)减小,所以电池负极区溶液的pH减小,故A错误;
B.Zn为负极,Ag2O为正极,电流由正极经外电路流向负极,故B正确;
C.Zn电极发生氧化反应,Ag2O电极发生还原反应,故C错误;
D.正极反应为Ag2O+H2O+2e=2Ag+2OH-,外电路中每通过0.2mol电子,则有0.1molAg2O反应,生成0.2molAg,正极的质量理论上减小1.6g,即O原子的质量,故D错误.
故选B.
B.Zn为负极,Ag2O为正极,电流由正极经外电路流向负极,故B正确;
C.Zn电极发生氧化反应,Ag2O电极发生还原反应,故C错误;
D.正极反应为Ag2O+H2O+2e=2Ag+2OH-,外电路中每通过0.2mol电子,则有0.1molAg2O反应,生成0.2molAg,正极的质量理论上减小1.6g,即O原子的质量,故D错误.
故选B.
点评:本题考查原电池的工作原理,为高频考点,侧重学生的分析能力的考查,明确电极反应、正负极的判断、电子的流向即可解答,题目难度不大.

练习册系列答案
相关题目
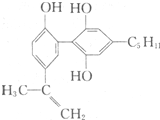 举办“人文奥运”的一个重要体现就是禁止运动员服用兴奋剂.有一种兴奋剂的结构简式如图,下列有关该物质的说法正确的是( )
举办“人文奥运”的一个重要体现就是禁止运动员服用兴奋剂.有一种兴奋剂的结构简式如图,下列有关该物质的说法正确的是( )| A、该分子中所有碳原子一定共存于同一平面中 |
| B、1 mol该物质与足量浓溴水反应时,至少消耗4 molBr2 |
| C、该物质属于苯酚同系物,则其遇FeCl3溶液一定显色 |
| D、由于该物质能使酸性KMn04溶液褪色,即可证明其分子必存在碳碳双键 |
常温下,现有1mL c1 mol/L的醋酸溶液和1mL c2mol/L的氢氧化钠溶液.下列说法中正确的是( )
| A、若c1=c2,则醋酸溶液中的c(H+)与氢氧化钠溶液中的c(OH-)相同 |
| B、若醋酸溶液的pH=3,氢氧化钠溶液的pH=11,则醋酸溶液中的c(CH3COO-)与氢氧化钠钠溶液中的c(Na+)相同 |
| C、将醋酸溶液与氢氧化钠溶液混合,若c1=c2,则所得溶液的pH=7 |
| D、将醋酸溶液与氢氧化钠溶液混合,若所得混合溶液的pH=7,则混合液中c(CH3COO-)>c(Na+) |
下列说法正确的是( )
| A、将氯化铝溶液加热,蒸干后得到无水氯化铝固体 |
| B、向Fe(OH)3胶体通电,发现胶体向正极移动,根据电场的作用,我们可以得出,Fe(OH)3带负电 |
| C、23Na37Cl中的质子数和中子数之比7:8 |
| D、硝酸铝溶液中滴加少量的氢氧化钠生成Al(OH)3 |
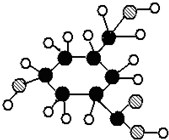
已知A物质的分子结构简式如图 ,lmol A与足量的NaOH溶液混合共热,充分反应后最多消耗NaOH的物质的量为( )
,lmol A与足量的NaOH溶液混合共热,充分反应后最多消耗NaOH的物质的量为( )
 ,lmol A与足量的NaOH溶液混合共热,充分反应后最多消耗NaOH的物质的量为( )
,lmol A与足量的NaOH溶液混合共热,充分反应后最多消耗NaOH的物质的量为( )| A、6mol | B、7mol |
| C、9mo1 | D、10mo1 |