题目内容
2.NA为阿伏伽德罗常数,下列物质所含原子数最多的是( )| A. | 0.8molCH4 | B. | 66gCO2 | ||
| C. | 标准状况下44.8L的O2 | D. | NA个水分子 |
分析 A.CH4的分子数带入N=n•NA计算,一个CH4分子含有5个原子;
B.由n=$\frac{m}{M}$、N=n•NA计算分子数,一个CO2分子含有3个原子;
C.由n=$\frac{V}{{V}_{m}}$、N=n•NA计算分子数,一个O2分子含有2个原子;
D.一个水分子含有3个原子.
解答 解:A.CH4的分子数N=0.8mol×NAmol-1=0.8NA,一个CH4分子含有5个原子,含有原子数为5×0.8NA=4NA,
B.n(CO2)=$\frac{66g}{44g/mol}$=1.5mol,N(CO2)=1.5mol×NAmol-1=1.5NA,原子数为3×1.5NA=4.5NA,
C.n(O2)=$\frac{44.8L}{22.4L/mol}$=2mol,N(O2)=2mol×NAmol-1=2NA,原子数为2×2NA=4NA,
D.一个水分子含有3个原子,NA个水分子含有3NA个原子,
因此含有原子数最多的是B,
故选B.
点评 本题考查物质的量有关计算,为高频考点,明确物质构成、物质的量公式中各个物理量关系即可解答,注意物质构成微粒,题目难度不大.

练习册系列答案
相关题目
12.下列有关原电池说法中正确的是( )
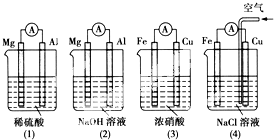

| A. | (1)(2)中活泼的Mg均作负极 | |
| B. | (2)中Mg作正极,电极反应式为6H2O+6e-=6OH-+3H2↑ | |
| C. | (3)中Fe作负极,电极反应式为Fe-2e-=Fe2+ | |
| D. | (4)中Cu作正极,电极反应式为2H++2e-=H2↑ |
10.下列有关化学实验的叙述正确的是( )
| A. | 为看到明显的实验现象,实验药品的取用越多越好 | |
| B. | 成功的化学实验必须严格遵守操作规程并取得预期成果,未取得预期成果的实验都是失败的 | |
| C. | 即使借助精密的仪器,采用规范的操作,化学实验依然会存在误差 | |
| D. | 为节约时间,保证实验顺利进行,应在所有的实验步骤都完成后再进行现象和数据的记录 |
17.在通常条件下,下列各组物质的性质排列正确的是( )
| A. | 熔点:CO2>KCl>SiO2 | B. | 水溶性:HCl>Cl2>CO2 | ||
| C. | 沸点:Cl2>Br2>I2 | D. | 热稳定性:HI>HBr>HCl |
7.给下列溶液中通入CO2气体,不可能产生沉淀的是( )
| A. | 氯化钙和硝酸钡的混合液 | B. | 水玻璃 | ||
| C. | 澄清石灰水溶液 | D. | 碳酸钠饱和溶液 |
14.下列实验操作中错误的是( )
| A. | 蒸发操作时,应使混合物中的水完全蒸干后,才能停止加热 | |
| B. | 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 分液操作时,分液漏斗中的下层液体从下口流出,上层液体从上口倒出 | |
| D. | 萃取操作时,溶质在萃取剂中的溶解度应大于在原溶剂中的溶解度 |
11.2011年3月日本地震引起福岛核反应堆事故,冷却反应堆需要大量的水,下列有关说法正确的是( )
| A. | H20分子中只含有非极性共价键 | |
| B. | H20分子中只含有极性共价键 | |
| C. | 水分子间只存在氢键 | |
| D. | 冷却反应堆用水在地球上常温下是固态 |
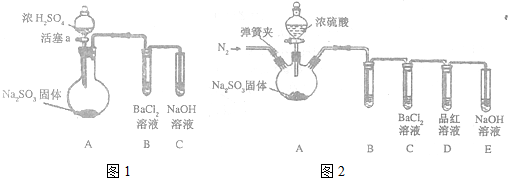
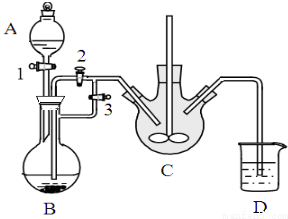 乳酸亚铁([CH3CH(OH)COO]2Fe•3H2O,M=288g/mol)是一种常用的补铁剂,可通过乳酸与碳酸亚铁反应制得:CH3CH(OH)COOH+FeCO3+2H2O→[CH3CH(OH)COO]2Fe•3H2O+CO2↑.
乳酸亚铁([CH3CH(OH)COO]2Fe•3H2O,M=288g/mol)是一种常用的补铁剂,可通过乳酸与碳酸亚铁反应制得:CH3CH(OH)COOH+FeCO3+2H2O→[CH3CH(OH)COO]2Fe•3H2O+CO2↑.