题目内容
实验室需要配制0.55mol?L-1 NaOH溶液220mL.
按下列操作步骤填上适当的文字,以使整个操作完整.
(1)选择仪器.完成本实验所必需的仪器有:托盘天平、药匙、烧杯、玻璃棒、 、 .
(2)计算.配制该溶液需取NaOH晶体 g.
(3)称量.
①天平调平后,应将天平的游码调至某个位置,请在如图中用一根竖线标出游码左边缘所处的位置:

②称量过程中NaOH晶体应放于天平的 (填“左盘”或“右盘”).
(4)溶解、冷却,该步实验中需要使用玻璃棒,目的是 .
(5)转移、洗涤.在转移时应使用玻璃棒引流,应注意 需要洗涤烧杯2~3次是为了 .
(6)定容、摇匀.
(7)将配好的溶液静置一段时间后,倒入指定的试剂瓶,贴好标签,注明溶液名称、浓度及配制的时间.
(8)下列操作使所配溶液浓度偏大的有 (填字母,下同);偏小的有 ;无影响的有 .
A、称量时用生锈的砝码
B、将NaOH放在纸上称量
C、NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中
D、往容量瓶转移时有少量液体溅出
E、未洗涤溶解NaOH的烧杯
F、定容时仰视刻度线
G、容量瓶未干燥就用来配制溶液.
按下列操作步骤填上适当的文字,以使整个操作完整.
(1)选择仪器.完成本实验所必需的仪器有:托盘天平、药匙、烧杯、玻璃棒、
(2)计算.配制该溶液需取NaOH晶体
(3)称量.
①天平调平后,应将天平的游码调至某个位置,请在如图中用一根竖线标出游码左边缘所处的位置:

②称量过程中NaOH晶体应放于天平的
(4)溶解、冷却,该步实验中需要使用玻璃棒,目的是
(5)转移、洗涤.在转移时应使用玻璃棒引流,应注意
(6)定容、摇匀.
(7)将配好的溶液静置一段时间后,倒入指定的试剂瓶,贴好标签,注明溶液名称、浓度及配制的时间.
(8)下列操作使所配溶液浓度偏大的有
A、称量时用生锈的砝码
B、将NaOH放在纸上称量
C、NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中
D、往容量瓶转移时有少量液体溅出
E、未洗涤溶解NaOH的烧杯
F、定容时仰视刻度线
G、容量瓶未干燥就用来配制溶液.
考点:配制一定物质的量浓度的溶液
专题:实验题
分析:(1)根据配制步骤是计算、称量、溶解、洗涤、定容、摇匀、装瓶来分析需要的仪器;
(2)根据n=cV和m=nM来计算;
(3)①根据需要称量的固体的质量来确定使用的砝码和游码的刻度;
②天平称量时应左物右码;
(4)溶解过程中,玻璃棒的作用是搅拌,加速溶解;
(5)用玻璃棒引流时应将玻璃棒末端插入到容量瓶的刻度线以下,且玻璃棒靠近容量瓶瓶口处不能接触瓶口;应考虑如果不洗涤烧杯,则会导致溶质的损失;
(8)根据c=
并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析;
(2)根据n=cV和m=nM来计算;
(3)①根据需要称量的固体的质量来确定使用的砝码和游码的刻度;
②天平称量时应左物右码;
(4)溶解过程中,玻璃棒的作用是搅拌,加速溶解;
(5)用玻璃棒引流时应将玻璃棒末端插入到容量瓶的刻度线以下,且玻璃棒靠近容量瓶瓶口处不能接触瓶口;应考虑如果不洗涤烧杯,则会导致溶质的损失;
(8)根据c=
| n |
| V |
解答:
(1)操作步骤有计算、称量、溶解、移液、洗涤移液、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解(可用量筒量取水加入烧杯),并用玻璃棒搅拌,加速溶解.冷却后转移到250mL容量瓶中,并用玻璃棒引流,洗涤烧杯、玻璃棒2-3次,并将洗涤液移入容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.所以所需仪器有托盘天平、药匙、烧杯、玻璃棒、250mL容量瓶、胶头滴管.
根据提供的仪器可知,还需仪器有250ml容量瓶、胶头滴管.
故答案为:250ml容量瓶、胶头滴管.
(2)由于无220ml的容量瓶,故应选用250ml的容量瓶,配制出250ml的溶液.根据n=cV可知需要的NaOH的物质的量n=0.55mol?L-1×0.25L=0.1375mol,质量m=nM=0.1375ml×40g/mol=5.5g,故答案为:5.5g;
(3)①根据需要称量的NaOH的质量是5.5g来确定使用5g的砝码和游码的刻度是0.5g,故游码的位置为: ,故答案为:
,故答案为: ;
;
②天平称量时应左物右码,故答案为:左盘;
(4)溶解过程中,玻璃棒的作用是搅拌,加速溶解,故答案为:搅拌,加速溶解;
(5)用玻璃棒引流时应将玻璃棒末端插入到容量瓶的刻度线以下,且玻璃棒靠近容量瓶瓶口处不能接触瓶口;如果不洗涤烧杯,则会导溶质的损失,故洗涤烧杯的目的是将溶质全部转移到容量瓶中.
故答案为:玻璃棒末端插入到容量瓶的刻度线以下,且玻璃棒靠近容量瓶瓶口处不能接触瓶口;将溶质全部转移到容量瓶中;
(8)A、砝码生锈后质量变大,故根据m物=m砝+m游,故称量出的药品的质量偏大,浓度偏大;
B、将NaOH放在纸上称量后容易潮解,导致NaOH的真实质量偏小,浓度偏小;
C、NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中,冷却后溶液体积偏小则浓度偏大;
D、往容量瓶转移时有少量液体溅出,会导致溶质的损失,则浓度偏小;
E、未洗涤溶解NaOH的烧杯,会导致溶质的损失,则浓度偏小;
F、定容时仰视刻度线,导致溶液体积偏大,浓度偏小;
G、若容量瓶未干燥即用来配制溶液,对溶液浓度无影响,因为只要定容时正确,至于水是原来就有的还是后来加入的,对浓度无影响;
故偏大的有:AC;偏小的有:BDEF;无影响的有:G.
根据提供的仪器可知,还需仪器有250ml容量瓶、胶头滴管.
故答案为:250ml容量瓶、胶头滴管.
(2)由于无220ml的容量瓶,故应选用250ml的容量瓶,配制出250ml的溶液.根据n=cV可知需要的NaOH的物质的量n=0.55mol?L-1×0.25L=0.1375mol,质量m=nM=0.1375ml×40g/mol=5.5g,故答案为:5.5g;
(3)①根据需要称量的NaOH的质量是5.5g来确定使用5g的砝码和游码的刻度是0.5g,故游码的位置为:
 ,故答案为:
,故答案为: ;
;②天平称量时应左物右码,故答案为:左盘;
(4)溶解过程中,玻璃棒的作用是搅拌,加速溶解,故答案为:搅拌,加速溶解;
(5)用玻璃棒引流时应将玻璃棒末端插入到容量瓶的刻度线以下,且玻璃棒靠近容量瓶瓶口处不能接触瓶口;如果不洗涤烧杯,则会导溶质的损失,故洗涤烧杯的目的是将溶质全部转移到容量瓶中.
故答案为:玻璃棒末端插入到容量瓶的刻度线以下,且玻璃棒靠近容量瓶瓶口处不能接触瓶口;将溶质全部转移到容量瓶中;
(8)A、砝码生锈后质量变大,故根据m物=m砝+m游,故称量出的药品的质量偏大,浓度偏大;
B、将NaOH放在纸上称量后容易潮解,导致NaOH的真实质量偏小,浓度偏小;
C、NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中,冷却后溶液体积偏小则浓度偏大;
D、往容量瓶转移时有少量液体溅出,会导致溶质的损失,则浓度偏小;
E、未洗涤溶解NaOH的烧杯,会导致溶质的损失,则浓度偏小;
F、定容时仰视刻度线,导致溶液体积偏大,浓度偏小;
G、若容量瓶未干燥即用来配制溶液,对溶液浓度无影响,因为只要定容时正确,至于水是原来就有的还是后来加入的,对浓度无影响;
故偏大的有:AC;偏小的有:BDEF;无影响的有:G.
点评:本题考查了一定物质的量浓度溶液的配制过程中的计算和误差分析,属于基础型题目,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列说法正确的是( )
| A、油脂是人体所需的基本营养物质之一,应尽量多食用油脂类物质 |
| B、糖尿病病人有糖分从尿液中排出,应多食用葡萄糖来补充 |
| C、营养物质并不是摄入越多越好,平时要注意膳食平衡 |
| D、高血压、高血脂的病人要尽量少食高脂肪食品 |
下列关于石油加工的叙述中,不正确的是( )
| A、石油分馏所得的馏分是一种具有固定熔沸点的纯净物 |
| B、石油裂化的主要目的是提高汽油等轻质油的产量 |
| C、石油裂解的原料是石油分馏产物,包括石油气 |
| D、石油在催化剂的作用下加热,可以使链状烃化为环状烃(如苯、甲苯) |
正确掌握化学用语是学好化学的基础.下列化学用语中正确的是( )
| A、乙烯的结构简式为CH2CH2 |
B、羟基的电子式: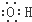 |
C、Ca2+的结构示意图为 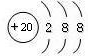 |
| D、乙醇的分子式:CH3CH2OH |
有机物①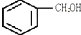 ②CH3CH2CH2OH ③CH≡C-CH2OH ④CH2=CH-COOCH3⑤CH2=CH-COOH中,既能发生加成反应和酯化反应,又能发生氧化反应的是( )
②CH3CH2CH2OH ③CH≡C-CH2OH ④CH2=CH-COOCH3⑤CH2=CH-COOH中,既能发生加成反应和酯化反应,又能发生氧化反应的是( )
 ②CH3CH2CH2OH ③CH≡C-CH2OH ④CH2=CH-COOCH3⑤CH2=CH-COOH中,既能发生加成反应和酯化反应,又能发生氧化反应的是( )
②CH3CH2CH2OH ③CH≡C-CH2OH ④CH2=CH-COOCH3⑤CH2=CH-COOH中,既能发生加成反应和酯化反应,又能发生氧化反应的是( )| A、③⑤ | B、①③⑤ | C、②④ | D、①③ |
已知A、B、C是中学化学的常见物质,它们在一定条件下有如下转化关系A
B
C,下列说法错误的是( )
| X |
| X |
| A、若A是一种淡黄色固体,B是造成酸雨的“罪魁祸首”,则X为O2 |
| B、若B与新制氢氧化铜共热,有砖红色沉淀生成,且C能使湿润的蓝色石蕊试纸变红,则A和C可以反应生成酯 |
| C、若B为两性氢氧化物,则C中一定存在Al3+ |
| D、A既可以为金属单质,也可以为非金属单质 |
少量锌和足量的稀HCl反应时,加入少量CuSO4固体,下列叙述正确的是( )
| A、反应速率减慢,产生H2的量不变 |
| B、反应速率加快,产生H2的量不变 |
| C、反应速率不变,产生H2的量略增加 |
| D、反应速率加快,产生H2的量略减少 |

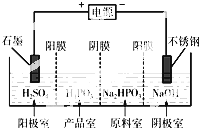
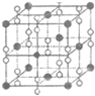 氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解.
氧元素和卤族元素都能形成多种物质,我们可以利用所学物质结构与性质的相关知识去认识和理解.