题目内容
4.25℃时,已知Ksp(Ag2S04)=1.2×10-5,Ksp(AgCl)=1.8×10-10,Ksp(AgC2O4)=3.5×10-11,Ksp(AgI)=1.5×10-16,该温度下有关叙述正确的( )| A. | AgCl、Ag2C2O4、AgI三者的饱和溶液中c(Ag+)大小顺序:Ag2C2O4>AgCl>AgI | |
| B. | 将0.02mol•L-1AgNO3溶液和0.02mol•L-1Na2SO4溶液等体积混合,有沉淀生成 | |
| C. | 向5mL饱和溶液AgCl溶液中滴加0.5mL0.1mol•L-1KI溶液,无沉淀生成 | |
| D. | 向浓度均为0.1mol•L-1的NaCl和KI混合溶液中滴加AgNO3溶液,先有白色沉淀生成 |
分析 A.根据Ag2C2O4、AgCl、AgI的Ksp计算;
B.当溶液中Qc(Ag2S04)>Ksp(Ag2S04)时,会生成沉淀;
C.溶度积小的沉淀已转化为溶解度更小的沉淀;
D.根据Ksp(AgCl)和Ksp(AgCl)判断,溶度积小的沉淀先生成.
解答 解:A.在Ag2C2O4饱和溶液中,Ksp(Ag2C2O4)=1.2×10-5 mol3•L-3=$\frac{1}{2}$c3(Ag+),因此c(Ag+)=2.88×10-2mol/L,
在AgCl饱和溶液中,Ksp(AgCl)=1.8×10-10 mol2•L-2=c(Ag+)•c(Cl-)=c2(Ag+),因此c(Ag+)≈1.34×10-5mol/L
在AgI饱和溶液中,Ksp(AgI)=8.3×10-17mol2/L-2=c(Ag+)•c(I-)=c2(Ag+),因此c(Ag+)≈9×10-8mol/L.
所以AgCl、Ag2C2O4、AgI三者的饱和溶液中c(Ag+)大小顺序:Ag2C2O4>AgCl>AgI,故A正确;
B.将0.02mol•L-1AgNO3溶液和0.02mol•L-1Na2SO4溶液等体积混合,c(Ag+)=0.01mol/L,c(SO42-)=0.01mol/L,则Qc=0.012×0.01=10-6<Ksp(Ag2SO4)=1.2×10-5,所以没有沉淀生成,故B错误;
C.已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16,溶度积小的沉淀已转化为溶解度更小的沉淀,所以向5mL饱和AgCl溶液中滴加0.5mL0.1mol•L-1KI溶液,会生成AgI沉淀,故C错误;
D.已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=1.5×10-16,溶度积小的沉淀先生成,所以向浓度均为0.1mol•L-1NaCl和KI混合溶液中滴加AgNO3溶液,先生成AgI沉淀,故D错误.
故选A.
点评 本题主要考查溶度积常数的概念和有关计算,题目难度中等,做题时注意不同物质的化学式是否相似,化学式相似的溶度积常数越小,溶液的浓度越小,侧重于考查学生的分析能力和计算能力.

①淀粉、纤维素、油脂、蛋白质都是天然有机高分子化合物
②淀粉、纤维素、蔗糖都属于糖类
③三大营养素糖类、油脂、蛋白质中,油脂是热能最高的营养素
④用纯碱( Na2CO3)热溶液洗涤餐具上的油污
⑤氯水使红墨水褪色原理和CH2=CH2使Br2的CCl4溶液褪色原理相同
⑥现用清洁燃料主要有压缩天然气和液化石油气两类,它们均属于碳氢化合物.
| A. | ①②③ | B. | ②③④⑥ | C. | ②④⑤⑥ | D. | ③④⑤ |
| A. | C4H8O2 | B. | C2H6O | C. | C4H10O2 | D. | C4H6O2 |
| A. | 将苯酚晶体放人少量水中,加热至全部溶解,冷却至50℃形成悬浊液 | |
| B. | 苯酚可以和硝酸发生取代反应 | |
| C. | 苯酚易溶于NaOH溶液中 | |
| D. | 苯酚的酸性比碳酸强,比醋酸弱 |
| A. | 0.1mol•L-1 | B. | 0.2mol•L-1 | C. | 0.5mol•L-1 | D. | 1mol•L-1 |
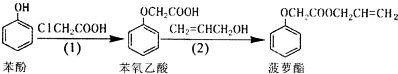
下列叙述错误的是( )
| A. | 苯酚和菠萝酯均可与酸性KMnO4溶液发生反应 | |
| B. | 苯酚、苯氧乙酸和菠萝酯均可与NaOH溶液发生反应 | |
| C. | 步骤(1)中由苯酚生成苯氧乙酸的反应属于取代反应 | |
| D. | 可用溴水检验步骤(2)的产物中是否有烯丙醇(CH2=CHCH2OH) 残留 |
| A. | 单质均能与水反应生成HXO | |
| B. | 从上到下,HX的氧化性增强,对应水溶液酸性增强 | |
| C. | 从上到下,卤素原子的电子层数依次增多,原子半径依次增大 | |
| D. | 卤素均能形成最高价含氧酸,其分子通式为HXO4 |
