题目内容
15.以下元素中,基态原子核外电子分布在7个不同能级的是( )| A. | N | B. | Cl | C. | Ti | D. | Br |
分析 根据各原子的电子轨道排布理论来回答,N原子核外电子排布为1s22s22p3,Cl原子核外电子排布为1s22s22p63s23p5,Ti原子核外电子排布为1s22s22p63s23p63d24s2,Br原子核外电子排布为1s22s22p63s23p64s24p5.
解答 解:A.N原子核外电子排布为1s22s22p3,有3个能级,故A错误;
B.Cl原子核外电子排布为1s22s22p63s23p5,有5个能级,故B错误;
C.Ti原子核外电子排布为1s22s22p63s23p63d24s2,共有7个能级,故C正确;
D.Br原子核外电子排布为1s22s22p63s23p63d104s24p5,有8个能级,故D错误.
故选:C.
点评 本题考查了原子的能级问题,题目难度不大,注意把握核外的排布规律以电子排布式的书写原理.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
5.下列不属于天然高分子化合物的是( )
| A. | 淀粉 | B. | 纤维素 | C. | 油脂 | D. | 蛋白质 |
6.对于以下的转化过程,要加入氧化剂才能够实现的是( )
| A. | O2→H2O | B. | Fe2+→Fe3+ | C. | H2SO4→CuSO4 | D. | HNO3→NO2 |
3.常温下,pH=9的Ba(OH)2溶液与pH=12的KOH溶液,按4:1的体积比混合,则溶液中c(H+)为(mol•L-1)( )
| A. | $\frac{(4{×10}^{-9}+1{×10}^{-12})}{5}$ | B. | $\frac{(8{×10}^{-9}+1{×10}^{-12})}{5}$ | ||
| C. | 5×10-10 | D. | 5×10-12 |
10.下列有关钠和镁的说法中,不正确的是( )
| A. | 电解饱和食盐水可以得到氯气 | |
| B. | 金属钠在高温下能将TiCl4中的钛置换出来 | |
| C. | 金属镁燃烧后会发出耀眼的白光,因此常用来制造信号弹和焰火 | |
| D. | 金属镁着火,可用二氧化碳灭火 |
20.用Na2SO3溶液吸收硫酸工业尾气中的SO2,Na2SO3+5O2+H2O═2NaHSO3所得混合液可电解循环再生(A为阳离子交换膜;B为阴离子交换膜).相关物料的传输与转化关系如图.下列说法不正确的是( )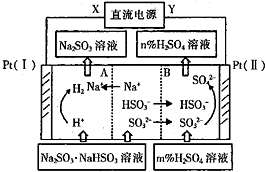

| A. | Pt(Ⅱ)为阳极 | B. | 阳极区[H+]增大 | ||
| C. | 图中的n<m | D. | 阴极电极反应式为2H++2e-═H2↑ |
4.下列叙述正确的是( )
| A. | 同温同压下,相同体积的物质,其物质的量一定相等 | |
| B. | 任何条件下,等物质的量的甲烷和一氧化碳所含的分子数一定相等 | |
| C. | 1L一氧化碳气体一定比1L氧气的质量小 | |
| D. | 相同条件下的一氧化碳气体和氨气,若体积相等,则原子数一定相等 |
5.25℃时,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | pH=12的溶液:K+、Na+、CH3COO-、ClO- | |
| B. | 0.1mol•L-1Na2CO3 溶液:K+、Ba2+、NO3-、Cl- | |
| C. | 0.1mol/LFeCl3溶液中:Al3+、NH4+、SCN-、SO42- | |
| D. | 使紫色石蕊试液变红的溶液:Fe2+、Mg2+、NO3-、SO42- |