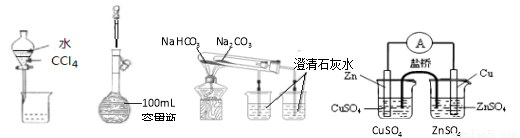
题目内容
下列说法正确的是( )
A.向Na2CO3溶液通入CO2,可使水解平衡:CO32 -+H2O HCO3- +OH-向正反应方向移动,则溶液pH增大
HCO3- +OH-向正反应方向移动,则溶液pH增大
B.室温时,0.1 mol·L-1某一元酸HA在水中有0.1%发生电离,则该溶液的pH=4
C.25 ℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.2NA
D.用玻璃棒蘸取溶液,点在湿润的pH试纸上测定其pH值
B
【解析】
试题分析:A、向Na2CO3溶液通入CO2,可使水解平衡:CO32 -+H2O HCO3- +OH-向正反应方向移动,最终生成碳酸氢钠,溶液的碱性降低,pH减小,A错误;B、室温时,0.1 mol·L-1某一元酸HA在水中有0.1%发生电离,则该溶液中氢离子浓度是0.1mol/L×0.1%=0.0001mol/L,则溶液的pH=4,B正确;C、25 ℃时,pH=13的1.0 L Ba(OH)2溶液中氢氧根的浓度是0.1mol/L,含有的OH-数目为0.1NA,C错误;D、pH试纸测定溶液pH值时,试纸不能事先润湿,D错误,答案选B。
HCO3- +OH-向正反应方向移动,最终生成碳酸氢钠,溶液的碱性降低,pH减小,A错误;B、室温时,0.1 mol·L-1某一元酸HA在水中有0.1%发生电离,则该溶液中氢离子浓度是0.1mol/L×0.1%=0.0001mol/L,则溶液的pH=4,B正确;C、25 ℃时,pH=13的1.0 L Ba(OH)2溶液中氢氧根的浓度是0.1mol/L,含有的OH-数目为0.1NA,C错误;D、pH试纸测定溶液pH值时,试纸不能事先润湿,D错误,答案选B。
考点:考查盐类水解、弱电解质的电离、阿伏伽德罗常数计算以及溶液pH测定

练习册系列答案
相关题目
下列根据实验操作和现象所得出的结论错误的是( )
选项 | 实验操作 | 实验现象 | 结论 |
A | 向硅酸钠溶液中滴加1滴酚酞,然后逐滴加入稀盐酸至红色褪去 | 2 min后,试管里 出现凝胶 | 酸性:盐酸>硅酸 |
B | 向蛋白质溶液中滴加饱和CuSO4溶液 | 有固体析出 | 蛋白质发生变性 |
C | 常温下,向浓硫酸中投入铁片 | 铁片不溶解 | 常温下,铁不与浓硫酸反应 |
D | 向某溶液中先滴加KSCN溶液,再滴加少量氯水 | 先无明显现象, 后溶液变成血红色 | 溶液中含有Fe2+,没有Fe3+ |
 KIO3+3H2↑。下列有关说法不正确的是 ( )
KIO3+3H2↑。下列有关说法不正确的是 ( )
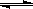 2Fe2O3?xH2O + 8H+,硫酸亚铁铵溶液较硫酸亚铁溶液不易被氧气氧化,其原因是 。
2Fe2O3?xH2O + 8H+,硫酸亚铁铵溶液较硫酸亚铁溶液不易被氧气氧化,其原因是 。