题目内容
能正确表示下列反应的离子方程式为( )
| A、碳酸氢钠溶液中滴入氢氧化钙溶液:HCO3-+OH-=CO32-+H2O |
| B、二氧化硫通入次氯酸钠溶液:SO2+ClO-+2OH-=SO42-+Cl-+H2O |
| C、硫化钡加入稀硫酸:BaS+2H+=H2S↑+Ba2+ |
| D、硅酸钠溶液与醋酸溶液混合:SiO32-+2H+=H2SiO3↓ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.氢氧化钙不足,离子方程式按照氢氧化钙的组成书写;
B.次氯酸钠过量,二氧化硫被氧化成硫酸钙离子;
C.硫化钡沉淀转化成硫酸钡沉淀,硫酸钡不能拆开;
D.醋酸为弱电解质,离子方程式中不能拆开,应该保留分子式.
B.次氯酸钠过量,二氧化硫被氧化成硫酸钙离子;
C.硫化钡沉淀转化成硫酸钡沉淀,硫酸钡不能拆开;
D.醋酸为弱电解质,离子方程式中不能拆开,应该保留分子式.
解答:
解:解:A.溶液中有钙离子,能与CO32-反应生成CaCO3,正确的离子方程式为:Ca2++2HCO3-+2OH-=CO32-+CaCO3↓+2H2O,故A错误;
B.ClO-具有强氧化性,能将二氧化硫氧化为硫酸根,离子方程式:SO2+ClO-+2OH-=SO42-+Cl-+H2O,故B正确;
C.Ba2+可与硫酸根反应生成硫酸钡沉淀,正确的离子方程式为:BaS+SO42-+2H+=H2S↑+BaSO4,故C错误;
D.醋酸酸性强于硅酸,反应生成硅酸和醋酸钠,醋酸为弱酸,不能拆开,正确的离子方程式为SiO32-+2CH3COOH=H2SiO3↓+2CH3COO-,故D错误;
故选B.
B.ClO-具有强氧化性,能将二氧化硫氧化为硫酸根,离子方程式:SO2+ClO-+2OH-=SO42-+Cl-+H2O,故B正确;
C.Ba2+可与硫酸根反应生成硫酸钡沉淀,正确的离子方程式为:BaS+SO42-+2H+=H2S↑+BaSO4,故C错误;
D.醋酸酸性强于硅酸,反应生成硅酸和醋酸钠,醋酸为弱酸,不能拆开,正确的离子方程式为SiO32-+2CH3COOH=H2SiO3↓+2CH3COO-,故D错误;
故选B.
点评:本题考查了离子方程式的正误判断,题目难度中等,注意明确离子方程式正误判断常用方法,如:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
相关题目
根据下列物质的名称,就能确认是纯净物的是( )
| A、溴乙烷 | B、二溴乙烷 |
| C、已烯 | D、二甲苯 |
下列微粒不属于官能团的是( )
| A、OH- |
| B、-Br |
| C、-COOH |
D、 |
下列各组气体通常情况下能大量共存,并且既能用浓硫酸干燥,又能用碱石灰干燥的是( )
| A、SO2、O2、HBr |
| B、H2、CH4、O2 |
| C、NH3、CO2、HCl |
| D、NH3、O2、N2 |
设NA为阿伏加德罗常数的值,下列有关说法正确的是( )
| A、1mol苯分子中含有C=C双键数为3NA | ||
| B、1mol甲基(-CH3)所含的电子总数为10NA | ||
C、标准状况下,1L甲醇完全燃烧后生成的CO2分子数目约为
| ||
| D、4.2g乙烯和丙烯的混合气体中所含碳原子数为0.3NA |
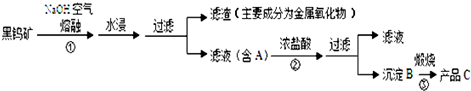
 除一种元素外,其余由元素周期表中前20号元素组成的物质A、B、C、D、E,它们间的反应关系如图:
除一种元素外,其余由元素周期表中前20号元素组成的物质A、B、C、D、E,它们间的反应关系如图: