题目内容
16.关于下列说法错误的是( )| A. | 0.7mol Na2O2与足量的CO2气体反应,电子转移0.7NA | |
| B. | 足量水蒸气与16.8gFe粉反应转移0.9mol电子 | |
| C. | Na与水、Al与NaOH溶液反应中水均作氧化剂 | |
| D. | 用钠从四氯化钛中置换钛,利用了钠的强还原性 |
分析 A.在2Na2O2+2CO2=2Na2CO3+O2中,过氧化钠中氧元素的化合价是-1价,碳酸钠中氧元素的化合价是-2价,氧气中氧元素的化合价是0价;
B.水蒸气与Fe反应生成Fe3O4;
C.Na与水、Al与NaOH溶液反应中水中的H元素的化合价降低;
D.Na是活泼金属,具有强还原性.
解答 解:A.在 2Na2O2+2CO2═2Na2CO3+O2反应中,只有Na2O2中O元素的化合价发生变化,分别由-1价变化为0价和-2价,由2Na2O2+2CO2=2Na2CO3+O2~2e-可知,生成1molO2时,转移的电子数为1mol×2=2mol,0.7mol Na2O2 与足量的CO2完全反应,转移电子的物质的量为0.7mol,故A正确;
B.水蒸气与Fe反应生成Fe3O4,16.8gFe粉的物质的量为$\frac{16.8g}{56g/mol}$=0.3mol,转移电子0.8mol,故B错误;
C.Na与水、Al与NaOH溶液反应中水中的H元素的化合价降低,所以反应中水为氧化剂,故C正确;
D.Na是活泼金属,具有强还原性,所以用钠从四氯化钛中置换钛,利用了钠的强还原性,故D正确.
故选B.
点评 本题考查了氧化还原反应,侧重于电子转移计算、氧化还原反应基本概念等知识点的考查,侧重于考查学生的分析能力和计算能力,题目难度中等.

练习册系列答案
相关题目
7.已知:2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ/mol.有关键能数据如下表:则水分子中O-H键能为( )
| 化学键 | H-H | O=O |
| 键能/kJ/mol | 436 | 498 |
| A. | 463.4kJ/mol | B. | 926.8kJ/mol | C. | 221.6kJ/mol | D. | 413kJ/mol |
4.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,16g O2和32g O3的混合物中,含有O原子数月为3NA | |
| B. | 标准状况下,1mol Na2O和1mol Na2O2的混合物中,含有离子总数为7NA | |
| C. | 1 mol NaBH4中离子键的数目为2NA | |
| D. | 在K${\;}_{\;}^{35}$ClO3+6H${\;}_{\;}^{37}$Cl═KCl+3Cl2↑+3H2O中,若生成71 g Cl2,转移的电子数目为$\frac{5}{3}$NA |
11.氮的氢化物NH3、N2H4等在工农业生产、航空航天等领域有广泛应用.
(1)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视.它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势.氨的燃烧实验涉及下列两个相关的反应:
①4NH3(g)+5O2(g)═4NO(g)+6H2O(l)△H1
②4NH3(g)+6NO(g)═5N2(g)+6H2O(l)△H2
则反应 4NH3(g)+3O2(g)═2N2(g)+6H2O(l)△H=$\frac{3△H{\;}_{1}+2△H{\;}_{2}}{5}$.(请用含有△H1、△H2的式子表示)
(2)合成氨实验中,在体积为3L的恒容密闭容器中,投入4mol N2和9mol H2在一定条件下合成氨,平衡时仅改变温度测得的数据如表所示:
已知:破坏1mol N2(g)和3mol H2(g)中的化学键吸收的总能量小于形成2mol NH3(g)中的化学键放出的总能量.①则T1<T2(填“>”、“<”或“=”)
②在T2时,经过10min达到化学平衡状态,则0至10min内H2的平均反应速率v(H2)=0.1mol•L-1•min-1,平衡时N2的转化率α(N2)=25%.
③下列图象分别代表焓变(△H)、混合气体平均相对分子质量($\overline{M}$)和气体密度(ρ)与反应时间的关系,其中正确且能表明该可逆反应达到平衡状态的是BC.

(1)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视.它在安全性、价格等方面较化石燃料和氢燃料有着较大的优势.氨的燃烧实验涉及下列两个相关的反应:
①4NH3(g)+5O2(g)═4NO(g)+6H2O(l)△H1
②4NH3(g)+6NO(g)═5N2(g)+6H2O(l)△H2
则反应 4NH3(g)+3O2(g)═2N2(g)+6H2O(l)△H=$\frac{3△H{\;}_{1}+2△H{\;}_{2}}{5}$.(请用含有△H1、△H2的式子表示)
(2)合成氨实验中,在体积为3L的恒容密闭容器中,投入4mol N2和9mol H2在一定条件下合成氨,平衡时仅改变温度测得的数据如表所示:
| 温度(K) | 平衡时NH3的物质的量(mol) |
| T1 | 2.4 |
| T2 | 2.0 |
②在T2时,经过10min达到化学平衡状态,则0至10min内H2的平均反应速率v(H2)=0.1mol•L-1•min-1,平衡时N2的转化率α(N2)=25%.
③下列图象分别代表焓变(△H)、混合气体平均相对分子质量($\overline{M}$)和气体密度(ρ)与反应时间的关系,其中正确且能表明该可逆反应达到平衡状态的是BC.

7.短周期五种非金属元素甲、乙、丙、丁、戊在元素周期表中的相对位置如图所示.下列判断正确的是( )
| 甲 | 乙 | |
| 丙 | 丁 | 戊 |
| A. | 原子半径:甲<乙,简单阴离子的半径:丙>丁>戊 | |
| B. | 非金属性:乙<丁 | |
| C. | 最高价氧化物对应的水化物的酸性:丙<丁 | |
| D. | 气态氢化物的稳定性:丙>丁>戊 |
4.对下列各溶液中,微粒的物质的量浓度关系表述正确的是( )
| A. | 0.1mol•L-1的(NH4)2SO4溶液中:c(SO42-)>c(NH4+)>c(H+)>c(OH-) | |
| B. | 0.1mol•L-1的NaHCO3溶液中:c(Na+)=c(HCO3-)+c(H2CO3)+2c(CO32-) | |
| C. | 0.1mol•L-1的氨水中:c(H+)=c(OH-) | |
| D. | 在25℃100mL NH4Cl溶液中:c(Cl-)=c(NH4+)+c(NH3•H2O) |
10. 在温度为373K时,将0.100mol无色的N2O4气体通入1L抽空的密闭容器中,立刻出现红棕色,直至建立N2O4?2NO2的平衡.如图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)
在温度为373K时,将0.100mol无色的N2O4气体通入1L抽空的密闭容器中,立刻出现红棕色,直至建立N2O4?2NO2的平衡.如图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)
(1)该反应在60S内用NO2的表示的反应速率为0.002 mol•L-1•s-1.
(2)下表是不同温度下测定得到的该反应的化学平衡常数.
据此可推测该反应(生成NO2)是吸热反应(填“吸热”或“放热”). 升高温度,平衡向正反应方向移动(填“正反应”或“逆反应”).
 在温度为373K时,将0.100mol无色的N2O4气体通入1L抽空的密闭容器中,立刻出现红棕色,直至建立N2O4?2NO2的平衡.如图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)
在温度为373K时,将0.100mol无色的N2O4气体通入1L抽空的密闭容器中,立刻出现红棕色,直至建立N2O4?2NO2的平衡.如图是隔一定时间测定到的N2O4的浓度(纵坐标为N2O4的浓度,横坐标为时间)(1)该反应在60S内用NO2的表示的反应速率为0.002 mol•L-1•s-1.
(2)下表是不同温度下测定得到的该反应的化学平衡常数.
| T/K | 323 | 373 |
| K值 | 0.022 | ? |
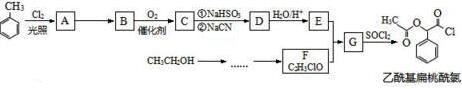
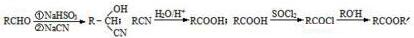
 .
. $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$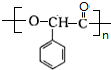 +nH2O.
+nH2O.