题目内容
 氯气是一种化学性质活泼的气体.
氯气是一种化学性质活泼的气体.(1)新制备的氯水呈
(2)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察的现象是
(3)为防止氯气污染空气,可用
考点:氯气的化学性质
专题:卤族元素
分析:(1)氯气微溶于水,与水反应:Cl2+H2O=H++Cl-+HClO;
(2)氯气本身不具有漂白性,可与水反应生成具有漂白性的HClO;
(3)氯气可与氢氧化钠反应,可用于吸收氯气.
(2)氯气本身不具有漂白性,可与水反应生成具有漂白性的HClO;
(3)氯气可与氢氧化钠反应,可用于吸收氯气.
解答:
解:(1)氯气微溶于水,水中因溶解少量氯气而呈黄绿色,氯气与水反应:Cl2+H2O=H++Cl-+HClO,氯水中有氯离子,加入AgNO3溶液,会有白色沉淀产生,反应的方程式为 AgNO3+HCl═AgCl↓+HNO3,
故答案为:黄绿色;氯气;白色沉淀; AgNO3+HCl═AgCl↓+HNO3;
(2)氯气本身不具有漂白性,可与水反应生成具有漂白性的HClO,可观察到的现象为干燥有色布条不退色,湿润有色布条退色,
故答案为:干燥有色布条不退色,湿润有色布条退色;
(3)氯气可与氢氧化钠反应,可用于吸收氯气,反应的方程式为Cl2+2NaOH=NaCl+NaClO+H2O,
故答案为:氢氧化钠; Cl2+2NaOH=NaCl+NaClO+H2O.
故答案为:黄绿色;氯气;白色沉淀; AgNO3+HCl═AgCl↓+HNO3;
(2)氯气本身不具有漂白性,可与水反应生成具有漂白性的HClO,可观察到的现象为干燥有色布条不退色,湿润有色布条退色,
故答案为:干燥有色布条不退色,湿润有色布条退色;
(3)氯气可与氢氧化钠反应,可用于吸收氯气,反应的方程式为Cl2+2NaOH=NaCl+NaClO+H2O,
故答案为:氢氧化钠; Cl2+2NaOH=NaCl+NaClO+H2O.
点评:本题综合考查元素化合物知识,侧重于氯气性质的考查,为高频考点,注意相关基础知识的积累,难度不大.

练习册系列答案
相关题目
 近来人们开发了通过电解同时生产NaOH和H2SO4的化学工艺,现在用离子交换膜(a、b)和石墨作电极的电解池进行生产NaOH和H2SO4,下列主产法中不正确的是( )
近来人们开发了通过电解同时生产NaOH和H2SO4的化学工艺,现在用离子交换膜(a、b)和石墨作电极的电解池进行生产NaOH和H2SO4,下列主产法中不正确的是( )| A、阴极反应式4OH--4e-=2H2O+O2↑ |
| B、阴极得到NaOH,阳极得到H2SO4 |
| C、每生产1molH2SO4,同时得到2mol NaOH |
| D、此反应实质就是电解水 |
下列实验操作正确的是( )
| A、用洁净的玻璃棒蘸取试液,点在湿润的pH 试纸上测定试液pH |
| B、在含有FeCl2杂质的FeCl3溶液中通入足量Cl2后,充分加热,除去过量的Cl2,即可得到纯净的FeCl3溶液 |
| C、用25mL 酸式滴定管量取18.00mL KMnO4溶液 |
| D、为减小中和滴定误差,锥形瓶必须洗净烘干并用待测液润洗后才能使用 |
某实验需要450ml 0.1mol/L的NaOH溶液,配制这种浓度的溶液时,下列有关说法正确的是( )
| A、配制时称量NaOH的质量(表达式)为:0.45 L×0.1 mol/L×40 g/mol |
| B、实际上需要配制的NaOH溶液为500mL |
| C、NaOH固体溶解后要立即将溶液转移至容量瓶中 |
| D、定容摇匀后,发现液面低于刻度线,应补水至液体凹液面与刻度线相切 |
钡和钠相似,也能形成O22-离子的过氧化物,下列叙述中正确的是( )
| A、过氧化钡的化学式为Ba2O2 |
| B、晶体中阴阳离子个数比为2:1 |
| C、1mol过氧化钡与足量水反应生成0.5mol氧气 |
| D、过氧化钠和过氧化钡都是强氧化剂 |
下面有关氯气的叙述正确的是( )
| A、氯气可使湿润的红布条退色,所以氯气具有漂白性 |
| B、在通常情况下,氯气可以和任何金属直接化合 |
| C、氯气没有漂白性,但通入品红溶液中,品红会退色 |
| D、氯气是黄绿色气体,闻其气味时要小心将集气瓶放在鼻孔下直接闻 |
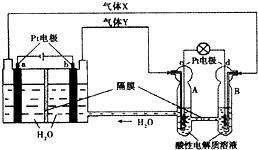 空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池.如图为RFC工作原理示意图,有关说法正确的是( )
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池.如图为RFC工作原理示意图,有关说法正确的是( )| A、当有0.2mol电子转移时,a极产生1.12L O2 |
| B、该装置开始工作后,右端装置能量变化为:电能→化学能 |
| C、d极上发生的电极反应是:O2+4H++4e一═2H2O |
| D、c极上进行还原反应,B中的H+可以通过隔膜进入A |
下列说法正确的是( )
| A、原子间的相互作用叫做化学键 |
| B、第三周期元素的最高正化合价等于它所处的主族序数 |
| C、VIIA 族元素阴离子的还原性越强,元素的最高价氧化物对应水化物的酸性也越强 |
| D、元素种类由质子数决定,元素原子的化学性质由最外层电子数决定 |
下列溶液中,Cl-的物质的量浓度与50mL1mol/LAlCl3溶液中Cl-物质的量浓度相等是( )
| A、100mL3mol/LKClO3溶液 |
| B、75mL2.5mol/LMgCl2溶液 |
| C、150mL3mol/LKCl溶液 |
| D、25mL2mol/LAlCl3溶液 |