题目内容
10.煤的干馏和石油的分馏都是物理变化.错.(判断对错)分析 根据化学变化是指在原子核不变的情况下,有新物质生成的变化,物理变化是指没有新物质生成的变化,化学变化与物理变化的本质区别在于是有无新物质生成解答.
解答 解:煤的干馏是将煤隔绝空气加强热使其分解生成煤焦油、煤气、焦炭等新物质的过程,该过程中有新物质生成,属于化学变化;
石油分馏是根据石油中各成分的沸点不同而分离的,变化过程中没有新物质生成,属于物理变化;
故答案为:错.
点评 本题考查物理变化与化学变化的区别,难度不大,解答时要分析变化过程中是否有新物质生成.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.己知金刚烷的结构如图所示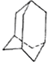 ,若有一个氯原子和一个溴原子取代它的两个氢原子,所得结构可能为( )
,若有一个氯原子和一个溴原子取代它的两个氢原子,所得结构可能为( )
 ,若有一个氯原子和一个溴原子取代它的两个氢原子,所得结构可能为( )
,若有一个氯原子和一个溴原子取代它的两个氢原子,所得结构可能为( )| A. | 7种 | B. | 8种 | C. | 9种 | D. | 10种 |
5.下列关于化学实验基本操作的叙述正确的是( )
| A. | 用托盘天平称量药品时,将药品置于天平右盘 | |
| B. | 蒸馏实验中,要在烧瓶中加入沸石或碎瓷片,以防止液体暴沸 | |
| C. | 将浓硫酸注入盛水的量筒中稀释 | |
| D. | 用蒸发皿进行加热蒸发操作时,必须垫石棉网 |
2.以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等.实验室模拟工业以硫酸渣制备铁红(Fe2O3),过程如图:
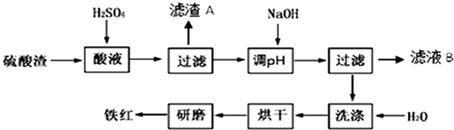
(1)硫酸渣的成分中既能与酸又能与碱反应的是Al2O3,写出酸溶过程Fe2O3与稀硫酸反应的离子反应方程式:Fe2O3+6H+═2Fe3++3H2O.
(2)生产过程中,为了确保铁红的纯度,氧化过程需要调节溶液的pH的范围是3.2-3.8(部分阳离子以氢氧化物形式沉淀时溶液的pH见表)
(3)滤渣A的主要成分为SiO2,滤液B含有的主要物质有Na2SO4、MgSO4、Al2(SO4)3.
(4)如何证明洗涤环节充分洗净取少许最后一次洗涤滤液,滴入1~2滴Ba(NO3)2溶液,若不出现白色浑浊,表示已洗涤完全.
(5)已知硫酸渣质量为a kg,假设铁红制备过程中铁元素损耗25%,最终得到铁红的质量为b kg,则原来硫酸渣中铁元素质量分数为$\frac{14b}{15a}$.(用题中所给数据计算并用最简整数比表示结果)

(1)硫酸渣的成分中既能与酸又能与碱反应的是Al2O3,写出酸溶过程Fe2O3与稀硫酸反应的离子反应方程式:Fe2O3+6H+═2Fe3++3H2O.
(2)生产过程中,为了确保铁红的纯度,氧化过程需要调节溶液的pH的范围是3.2-3.8(部分阳离子以氢氧化物形式沉淀时溶液的pH见表)
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀 | 2.7 | 3.8 | 7.5 | 9.4 |
| 完全沉淀 | 3.2 | 5.2 | 9.7 | 12.4 |
(4)如何证明洗涤环节充分洗净取少许最后一次洗涤滤液,滴入1~2滴Ba(NO3)2溶液,若不出现白色浑浊,表示已洗涤完全.
(5)已知硫酸渣质量为a kg,假设铁红制备过程中铁元素损耗25%,最终得到铁红的质量为b kg,则原来硫酸渣中铁元素质量分数为$\frac{14b}{15a}$.(用题中所给数据计算并用最简整数比表示结果)
19.以石墨为电极,电解下列等体积、等物质的量浓度的混合溶液,阴、阳两极收集到的气体体积可能相等的是( )
| A. | 硝酸银和氯化钠的混合溶液 | B. | 硫酸铜和硫酸钾的混合溶液 | ||
| C. | Na2CO3和NaOH混合溶液 | D. | CuCl2和HCl混合溶液 |
20.下列相关实验或现象的描述正确的是( )
| A. | 甲烷中混有的乙烯,可以用酸性KMnO4溶液洗气除去 | |
| B. | 乙烯、苯都易燃烧,燃烧时都产生明亮火焰、大量黑烟 | |
| C. | 乙酸乙酯、油脂都能水解,且在热的NaOH溶液中水解更完全 | |
| D. | 葡萄糖、淀粉都有还原性,都能与新制Cu(OH)2共热产生砖红色沉淀 |
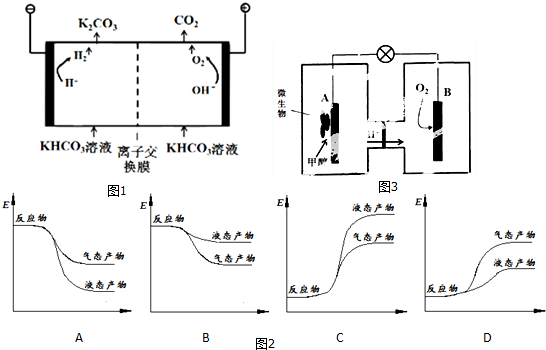
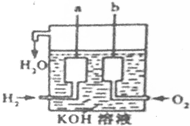 (1)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如图所示:a、b两个电极均由多孔的碳块组成.写出b极的电极反应方程式.工作时电池负极区的pH减小(填“增大”、“减小”或“不变”).
(1)美国阿波罗宇宙飞船上使用了一种新型装置,其构造如图所示:a、b两个电极均由多孔的碳块组成.写出b极的电极反应方程式.工作时电池负极区的pH减小(填“增大”、“减小”或“不变”).