题目内容
【题目】燃煤厂为减少SO2的排放,可采取的措施是:
①洗涤含SO2的烟气,下列物质可作洗涤剂的是 .
a.浓NH3H2O b.NaHCO3 c.FeCl3 d.NaHSO3
②将煤转化为清洁气体燃料,过程如图所示: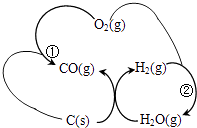
已知:反应①生成1molCO(g)的反应热△H=﹣110.5KJ/mol反应②生成1molH2O(g)的反应热△H=﹣241.6KJ/mol焦炭与水蒸气反应的热化学方程式是 .
【答案】abc;C(s)+H2O(g)=CO(g)+H2(g)△H=+131.1 kJ?mol﹣1
【解析】解:①洗涤含SO2的烟气,根据酸性氧化物的性质可选,
a.浓NH3H2O和二氧化硫反应可以吸收二氧化硫,故A字裙;
b.NaHCO3 溶液和二氧化硫反应可以吸收二氧化硫气体,故b正确;
c.FeCl3 溶液和二氧化硫发生氧化还原反应,可以吸收二氧化硫,故c正确;
d.NaHSO3不能和二氧化硫发生反应,不能吸收二氧化硫,故d错误;
所以答案是:abc;②反应①热化学方程式为:①C(s)+ ![]() O2(g)=CO(g)△H=﹣110.5KJ/mol,反应②的热化学方程式为:②H2(g)+
O2(g)=CO(g)△H=﹣110.5KJ/mol,反应②的热化学方程式为:②H2(g)+ ![]() O2(g)=H2O(g)△H=﹣241.6KJ/mol
O2(g)=H2O(g)△H=﹣241.6KJ/mol
依据盖斯定律计算①﹣②得到C(s)+H2O(g)=CO(g)+H2(g)△H=+131.1 kJmol﹣1 ,
所以答案是:C(s)+H2O(g)=CO(g)+H2(g)△H=+131.1 kJmol﹣1 .

练习册系列答案
相关题目