题目内容
根据元素在元素周期表中的相对位置,判断下列化合物中,化学键极性最大的是( )
| A、H2S |
| B、CH4 |
| C、NH3 |
| D、H2O |
考点:极性键和非极性键
专题:元素周期律与元素周期表专题,化学键与晶体结构
分析:根据成键原子的电负性之差判断,电负性差值越大,则键的极性越大.
解答:
解:电负性差值越大,则键的极性越大,同周期从左到右电负性逐渐增大,同主族从上到下电负性逐渐减小,在周期表中距离越远,则电负性差别越大,则电负性差别最大的为H和O,所以化学键极性最大的是H2O;
故选D.
故选D.
点评:本题考查了化学键极性的比较,注意把握其判断方法,从电负性的角度考虑,题目难度不大.

练习册系列答案
相关题目
气体的体积主要由以下什么因素决定( )
①气体分子的直径 ②气体的物质的量 ③气体分子间的平均距离.
①气体分子的直径 ②气体的物质的量 ③气体分子间的平均距离.
| A、①② | B、①③ | C、②③ | D、①②③ |
下列卤代烃发生消去后,可以得到两种烯烃( )
| A、1-氯丁烷 |
| B、2-甲基-2-氯丙烷 |
| C、3,3-二甲基-2-氯丁烷 |
| D、2-甲基-2-溴戊烷 |
具有下列电子排布式的原子中,半径最大的是( )
| A、ls22s22p63s23p5 |
| B、1s22s22p3 |
| C、1s22s22p2 |
| D、1s22s22p63s23p4 |
两种金属混合粉末15g,与足量的盐酸反应恰好生成11.2L氢气(标准状况),符合上述情况的金属混合物为( )
| A、Mg和Al |
| B、Fe和Zn |
| C、Cu和Zn |
| D、Mg和Ag |
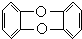 ,其中苯环上的氢原子如果被氯原子取代,所得到的物质有剧毒.当两个氯原子取代苯环上的氢时,所得的异构体数是( )
,其中苯环上的氢原子如果被氯原子取代,所得到的物质有剧毒.当两个氯原子取代苯环上的氢时,所得的异构体数是( ) 有机物键线式结构的特点是以线示键,每个折点和线端点处表示有一个碳原子,并以氢补足四价,C、H不表示出来.降冰片烷立体结构如图所示:
有机物键线式结构的特点是以线示键,每个折点和线端点处表示有一个碳原子,并以氢补足四价,C、H不表示出来.降冰片烷立体结构如图所示: