题目内容
已知反应:CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41kJ?mol-1和2H2(g)+O2(g)═2H2O(g)△H=-484kJ?mol-1.则下列说法不正确的是( )
| A、CO转化为CO2的热化学方程式为2CO(g)+O2(g)═2CO2(g)△H=-566 kJ?mol-1 | ||
B、CO燃烧热的热化学方程式为CO(g)+
| ||
| C、放热反应可能需要加热才能进行,而吸热反应一定需要加热才能进行 | ||
| D、1mol H2完全燃烧生成1mol 液态水,放出的热量大于242 kJ |
考点:有关反应热的计算
专题:
分析:A.根据已知方程式由盖斯定律分析;
B.根据1molCO完全燃烧放出的热量来书写;
C.很多放热反应也需要反应条件;
D.气态水转化为液态水会放热.
B.根据1molCO完全燃烧放出的热量来书写;
C.很多放热反应也需要反应条件;
D.气态水转化为液态水会放热.
解答:
解:A.已知反应:CO(g)+H2O(g)═CO2(g)+H2(g)△H=-41kJ?mol-1和2H2(g)+O2(g)═2H2O(g)△H=-484kJ?mol-1第一个方程式的计量数乘以2,再与第二个相加得:2CO(g)+O2(g)═2CO2(g)△H=-566 kJ?mol-1,故A正确;
B.由A项2CO(g)+O2(g)═2CO2(g)△H=-566 kJ?mol-1,可知1molCO完全燃烧放出的热量为283 kJ,则CO燃烧热的热化学方程式为CO(g)+
O2(g)═CO2(g)△H=-283 kJ?mol-1,故B正确;
C.很多放热反应也需要反应条件,如CO的燃烧需要点燃,吸热反应不一定需要加热才能进行如氢氧化钡晶体与氯化铵晶体常温下能反应,故C错误;
D.气态水转化为液态水会放热,所以1mol H2完全燃烧生成1mol 液态水,放出的热量大于242 kJ,故D正确.
故选C.
B.由A项2CO(g)+O2(g)═2CO2(g)△H=-566 kJ?mol-1,可知1molCO完全燃烧放出的热量为283 kJ,则CO燃烧热的热化学方程式为CO(g)+
| 1 |
| 2 |
C.很多放热反应也需要反应条件,如CO的燃烧需要点燃,吸热反应不一定需要加热才能进行如氢氧化钡晶体与氯化铵晶体常温下能反应,故C错误;
D.气态水转化为液态水会放热,所以1mol H2完全燃烧生成1mol 液态水,放出的热量大于242 kJ,故D正确.
故选C.
点评:本题考查了反应热的计算、盖斯定律的应用、热化学方程式的书写等,题目难度不大,注意把握盖斯定律的原理和应用.

练习册系列答案
相关题目
下列有关电解质的说法中正确的是( )
| A、物质的量相同的磷酸钠溶液和磷酸溶液中所含PO43-的量相同 | ||
B、将NaOH和氨水溶液各稀释一倍,两者OH-浓度均减少到原的
| ||
| C、强电解质溶液的导电能力不一定比弱电解质溶液强 | ||
| D、如果盐酸的浓度是醋酸浓度的二倍,则盐酸中c(H+)也是醋酸中c(H+)的二倍 |
下列离子反应方程式正确的是( )
| A、金属铁与稀硫酸反应 2Fe+6H+=2Fe3++3H2↑ |
| B、NaHCO3与盐酸:HCO3-+H+=H2O+CO2↑ |
| C、碳酸钡与盐酸反应 CO32-+2H+═H2O+CO2↑+Ba2+ |
| D、醋酸与小苏打溶液反应H++HCO3-=CO2↑+H2O |
下列离子方程式正确的是( )
| A、碳酸钡与足量盐酸反应:2H++BaCO3=Ba2++H2O+CO2↑ |
| B、氯气通入蒸馏水中:Cl2+H2O=Cl-+ClO-+2H+ |
| C、氢氧化钡溶液与稀硫酸混合:Ba2++SO42-+H++OH-=BaSO4↓+H2O |
| D、过量CO2通入澄清石灰水中:CO2+Ca(OH)2=CaCO3↓+H2O |
已知2Fe2++Br2=2Fe3++2Br-.向100mL的FeBr2溶液中通入标准状况下的Cl23.36L,充分反应后测得溶液中Cl-与Br-的物质的量浓度相等,则原FeBr2溶液的物质的量浓度为( )
| A、2 mol/L |
| B、1 mol/L |
| C、0.4 mol/L |
| D、0.2 mol/L |
甲烷和丙烷混合气的密度与同温同压下一氧化碳的密度相同,混合气中甲烷和丙烷的体积比是( )
| A、4:3 | B、3:4 |
| C、2:1 | D、1:1 |
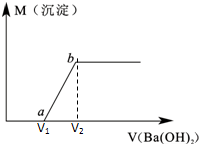 某溶液由盐酸、Na2CO3、H2SO4、CuCl2四种物质中的一种或几种混合形成,现向该混合溶液中滴加Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液体积的关系如图所示.
某溶液由盐酸、Na2CO3、H2SO4、CuCl2四种物质中的一种或几种混合形成,现向该混合溶液中滴加Ba(OH)2溶液,产生沉淀的质量与加入Ba(OH)2溶液体积的关系如图所示.