题目内容
下图是周期表中短周期的一部分,A、B、C三种元素的原子核外电子数之和等于B的质量数的2.5倍,B元素的原子核内质子数等于中子数,下列叙述不正确的是( )
| B | ||
| A | C |
| A、A为ⅤA族元素 |
| B、B为第二周期的元素 |
| C、C是周期表中化学性质最活泼的非金属 |
| D、三种元素都为非金属元素 |
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:根据A、B、C三种元素在周期表中的位置可知,B位于第二周期,A、C位于第三周期,设B的核外电子总数为x,B的核电荷数=质子数=x,B元素的原子核内质子数等于中子数,则B的质量数为2x;
则A的核外电子数=原子序数=x+8-1,C的最外层电子数为x+8+1,A、B、C三种元素的原子核外电子数之和等于B的质量数的2.5倍,则:x+(x+8-1)+(x+8+1)=2.5×2x,解得:x=8,则B为O元素、A为P元素、C为Cl元素,然后联系元素周期表、元素周期律知识对各选项进行判断.
则A的核外电子数=原子序数=x+8-1,C的最外层电子数为x+8+1,A、B、C三种元素的原子核外电子数之和等于B的质量数的2.5倍,则:x+(x+8-1)+(x+8+1)=2.5×2x,解得:x=8,则B为O元素、A为P元素、C为Cl元素,然后联系元素周期表、元素周期律知识对各选项进行判断.
解答:
解:根据图示及元素周期表结构可知,B位于第二周期,A、C位于第三周期,设B的核外电子总数为x,B的核电荷数=质子数=x,B元素的原子核内质子数等于中子数,则B的质量数为2x;则A的核外电子数=原子序数=x+8-1,C的最外层电子数为x+8+1,A、B、C三种元素的原子核外电子数之和等于B的质量数的2.5倍,则:x+(x+8-1)+(x+8+1)=2.5×2x,解得:x=8,则B为O元素、A为P元素、C为Cl元素,
A.A为P元素,原子序数为15,位于周期表中第三周期第ⅤA族,故A正确;
B.B为O元素,原子序数为8,位于周期表中第二周期第ⅥA族,故B正确;
C.C为Cl元素,周期表中化学性质最活泼的非金属为F元素,故C错误;
D.根据分析可知,B为O元素、A为P元素、C为Cl元素,三者都是非金属元素,故D正确;
故选C.
A.A为P元素,原子序数为15,位于周期表中第三周期第ⅤA族,故A正确;
B.B为O元素,原子序数为8,位于周期表中第二周期第ⅥA族,故B正确;
C.C为Cl元素,周期表中化学性质最活泼的非金属为F元素,故C错误;
D.根据分析可知,B为O元素、A为P元素、C为Cl元素,三者都是非金属元素,故D正确;
故选C.
点评:本题考查了位置结构与性质的关系,题目难度中等,正确推断元素名称为解答关键,注意掌握原子结构与元素周期表、元素周期律的关系,试题有利于培养学生的分析、理解能力及灵活应用所学知识的能力.

练习册系列答案
相关题目
分子式为C9H12的所有带苯环结构的异构体中,在催化剂条件下与液溴发生取代反应,其一溴代物为三种的结构有( )
| A、1种 | B、2种 | C、3种 | D、4种 |
把Ca(OH)2放入蒸馏水中,一定时间后达到如下平衡:Ca(OH)2(s)?Ca2+(aq)+2OH-(aq),加入以下固体,能使Ca(OH)2减少的是( )
| A、NaOH |
| B、Na2CO3 |
| C、CaCl2 |
| D、NaClO |
对于反应2A(g)+B(g)?2C(g)△H<0,下列图象正确的是( )


| A、①④ | B、②③ | C、①③ | D、②④ |
一种从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的工艺流程如下下列说法中正确的是( )
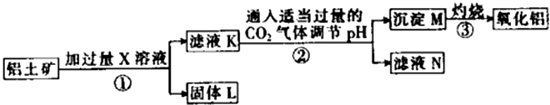

| A、X既可以是HCl,也可以是NaOH |
| B、第②步反应的离子方程式为2AlO2-+CO2+3H2O═2Al(OH)3↓+CO32- |
| C、固体L中含有Fe2O3和MgO等 |
| D、滤液N经蒸干、灼烧后可以得到纯净的Na2CO3固体 |