题目内容
为了测定某铜银合金的成分,将30.0g合金溶于80mL13.5mol/L的浓硝酸中,待合金完全溶解后,收集到6.72L(标准状况)NO和NO2的混合气体,并测得溶液中H+浓度为1mol/L.假设反应后溶液的体积仍为80mL,试计算.
(1)被还原硝酸的物质的量.
(2)合金中银的质量分数.
(1)被还原硝酸的物质的量.
(2)合金中银的质量分数.
考点:有关混合物反应的计算
专题:
分析:(1)被还原的硝酸生成NO2或NO2、NO混合物,根据N元素守恒计算被还原硝酸的物质的量;
(2)设混合物中Cu、Ag物质的量分别为xmol、ymol,产物Cu(NO3)2、AgNO3中含NO3-物质的量各为2xmol、ymol,根据合金质量及N原子守恒列方程,再根据m=nM计算Ag的质量,进而计算合金中银的质量分数.
(2)设混合物中Cu、Ag物质的量分别为xmol、ymol,产物Cu(NO3)2、AgNO3中含NO3-物质的量各为2xmol、ymol,根据合金质量及N原子守恒列方程,再根据m=nM计算Ag的质量,进而计算合金中银的质量分数.
解答:
解:(1)被还原的硝酸生成NO2或NO2、NO混合物,根据N元素守恒,故被还原的n(HNO3)=n(气体)=6.72 L÷22.4L/mol=0.3mol,
答:被还原的硝酸的物质的量为0.3mol;
(2)反应的n(HNO3)=13.5 mol/L×0.08L-1 mol/L×0.08L=1 mol
设合金中铜、银物质的量分别为xmol、ymol,则:64x+108y=30
产物Cu(NO3)2、AgNO3中含NO3-物质的量各为2x mol、y mol,据N守恒可得:2x+y+0.3=1
联立方程,解得:x=0.3、y=0.1,
故合金中银的质量为:0.1 mol×108g/mol=10.8g,
合金中Ag的质量分数为:
×100%=36%,
答:合金中银的质量质量分数为36%.
答:被还原的硝酸的物质的量为0.3mol;
(2)反应的n(HNO3)=13.5 mol/L×0.08L-1 mol/L×0.08L=1 mol
设合金中铜、银物质的量分别为xmol、ymol,则:64x+108y=30
产物Cu(NO3)2、AgNO3中含NO3-物质的量各为2x mol、y mol,据N守恒可得:2x+y+0.3=1
联立方程,解得:x=0.3、y=0.1,
故合金中银的质量为:0.1 mol×108g/mol=10.8g,
合金中Ag的质量分数为:
| 10.8g |
| 30g |
答:合金中银的质量质量分数为36%.
点评:本题考查混合物反应的计算、氧化还原反应计算,题目难度中等,明确反应中硝酸起氧化剂、还原剂作用为解答关键,注意掌握质量守恒在化学计算中的应用方法.

练习册系列答案
相关题目
物质的提纯是化学实验中的一项重要操作,也是化工生产及物质制备中的主要环节.下列有关叙述中不正确的是( )
| A、乙酸乙酯中混有乙酸,可选用饱和Na2CO3溶液洗涤,然后将两层液体分开 |
| B、在提纯鸡蛋中的蛋白质时,可向鸡蛋清溶液中加入浓(NH4)2SO4溶液,然后将所得沉淀滤出,即得较纯的蛋白质 |
| C、油脂提纯中,可将油脂加入浓NaOH溶液中加热,然后过滤,滤出的溶液即为较纯的油脂 |
| D、甘蔗是制备蔗糖的主要原料,榨出的甘蔗汁因含色素而呈棕黄色,在制取蔗糖前应先加入适量的活性炭,搅拌、过滤、蒸发结晶,即得较纯的蔗糖 |
1mol甲烷完全和氯气发生取代反应,生成四种取代产物的 物质的量相同,那么消耗氯气的物质的量为( )
| A、0.5mol |
| B、2mol |
| C、2.5mol |
| D、4mol |
氢化铵(NH4H)与氯化铵的结构相似,又知NH4H与水反应有H2生成,下列叙述不正确的是( )
| A、NH4H是离子化合物 |
| B、NH4H中含有离子键和共价键 |
| C、NH4H与水反应时,NH4H是氧化剂 |
| D、NH4H固体溶于水形成的溶液显碱性 |

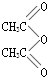
 +AS
+AS +CH2COOH
+CH2COOH
 与NaOH的醇溶液共热制备CH3-CH═CH2
与NaOH的醇溶液共热制备CH3-CH═CH2