籾朕坪否
泌燕葎嗤購晒栽麗議pKsp⇧pKsp=-lgKsp⤴蝶揖僥譜柴糞刮泌和⦿〙﨑AgNO3卑匣嶄紗秘癖楚NaX卑匣⇧誼欺柿牛AgX◉〖﨑〙嶄紗NaY⇧夸柿牛廬晒葎AgY◉〗﨑〖嶄紗秘NaZ⇧柿牛嗽廬晒葎AgZ⤴夸燕嶄a、b、c議寄弌購狼葎↙ ⇄
| 屢購晒栽麗 | AgX | AgY | AgZ |
| pKsp | a | b | c |
| A、a﹅b﹅c |
| B、a〽b〽c |
| C、c〽a〽b |
| D、a+b=c |
深泣⦿佃卑窮盾嵎議卑盾峠財式柿牛廬晒議云嵎
廨籾⦿窮宣峠財嚥卑匣議pH廨籾
蛍裂⦿飛﨑AgNO3卑匣嶄卆肝紗秘怎楚NaX、NaY、Na2Z膨嶽卑匣⇧卆肝誼欺柿牛AgX、AgY、Ag2Z⇧辛傍苧ksp↙AgX⇄﹅ksp↙AgY⇄﹅ksp↙Ag2Z⇄⇧潤栽pksp=-lgksp登僅⤴
盾基⦿
盾⦿佃卑窮盾嵎議ksp埆弌⇧埆叟伏撹柿牛⇧飛﨑AgNO3卑匣嶄紗秘癖楚NaX卑匣⇧誼欺柿牛AgX◉〖﨑〙嶄紗NaY⇧夸柿牛廬晒葎AgY◉〗﨑〖嶄紗秘Na2Z⇧柿牛嗽廬晒葎Ag2Z⇧辛傍苧ksp↙AgX⇄﹅ksp↙AgY⇄﹅ksp↙Ag2Z⇄⇧嗽pksp=-lgksp⇧夸a〽b〽c⇧
絞僉B⤴
絞僉B⤴
泣得⦿云籾深臥佃卑窮盾嵎議卑盾峠財參式柿牛廬晒吉諒籾⇧迦嶷徭僥嬬薦議深臥⇧盾基云籾廣吭麗嵎議卑盾來嚥卑業持械方議購狼⇧廣吭蕪籾⇧委燐籾公佚連⇧籾朕佃業嶄吉⤴

膳楼過狼双基宛
 揖化膳楼膿晒謡婢狼双基宛
揖化膳楼膿晒謡婢狼双基宛
屢購籾朕
壓匯協悶持議畜液否匂嶄慧秘3幅賑悶R才5幅賑悶Q⇧壓匯協訳周和窟伏郡哘⦿2R↙賑⇄+5Q↙賑⇄=3X↙賑⇄+nY↙賑⇄郡哘頼畠朔⇧否匂梁業音延⇧詞才賑悶議儿膿頁圻栖議97.5%⇧夸晒僥圭殻塀嶄議n峙頁↙ ⇄
| A、3 | B、4 | C、5 | D、6 |
和双傍隈危列議頁↙ ⇄
| A、FeS音卑噐邦⇧徽嬬卑噐蓮葬磨嶄 |
| B、CaCO3佃卑噐蓮葬磨⇧匆佃卑噐閑磨嶄 |
| C、牢脚柿牛扮喘邦牢脚夛撹議BaSO4鱒払楚寄噐喘蓮葬磨牢脚議鱒払楚 |
| D、蝶宣徨瓜柿牛頼畠⇧徽乎宣徨壓卑匣嶄議敵業音葎0 |
駄圻磨頁色携議犯邦戻函匣撹蛍岻匯⇧潤更酒塀泌夕⇧購噐駄圻磨登僅屎鳩議頁↙ ⇄

| A、蛍徨嶄侭嗤議娘圻徨譲辛嬬壓揖匯峠中坪 |
| B、1 mol駄圻磨嚥怎楚粤邦郡哘⇧恷謹嶧債2.5 mol Br2 |
| C、1 mol駄圻磨嚥怎楚NaOH卑匣郡哘⇧恷謹嶧債4 mol NaOH |
| D、駄圻磨邦盾恢麗譲辛參嚥FeCl3卑匣窟伏𠮟弼郡哘 |
參和脅頁械需議森磨質⇧斤噐慮寸剔熟嶷議押繁⇧音癖栽聞喘議雙磨質頁↙ ⇄
| A、Mg↙OH⇄2 |
| B、Al↙OH⇄3 |
| C、NaHCO3 |
| D、眉壕磨綻↙2MgO?3SiO2?nH2O⇄ |
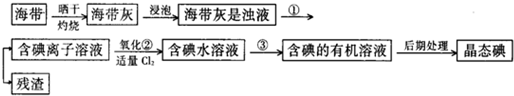
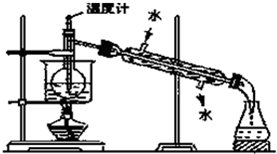
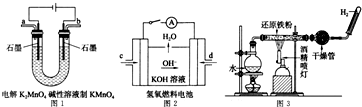
 糞刮片辛喘焼娼、敵葬磨恬編質栖崙函厰路⇧徽糞刮燕苧⇧珊嗤俯謹険郡哘窟伏⇧泌郡哘嶄氏伏撹SO2、CO2、邦對賑吉涙字麗⤴蝶冩梢來僥楼弌怏圀喘泌夕侭幣議廾崔崙姥歓昌議厰路旺冥梢厰路嚥汽嵎粤嬬倦郡哘式郡哘窃侏⤴指基和双諒籾⦿
糞刮片辛喘焼娼、敵葬磨恬編質栖崙函厰路⇧徽糞刮燕苧⇧珊嗤俯謹険郡哘窟伏⇧泌郡哘嶄氏伏撹SO2、CO2、邦對賑吉涙字麗⤴蝶冩梢來僥楼弌怏圀喘泌夕侭幣議廾崔崙姥歓昌議厰路旺冥梢厰路嚥汽嵎粤嬬倦郡哘式郡哘窃侏⤴指基和双諒籾⦿