题目内容
(10分)某化学课外活动小组将氯化钠固体中混有的硫酸钠、碳酸氢铵杂质除去并得到氯化钠溶液,设计了如下方案:

(1)操作①的目的是: ;
(2)操作②是否可改为加硝酸钡溶液?为什么? ;
(3)进行操作②后,如何判断SO42-已除尽,方法是: ;
(4)在操作③中为什么不在加Na2CO3溶液之前先过滤?理由是: ;
(5)操作④的目的是: 。
(1)除去NH4HCO3,NH4HCO3 ==NH3↑+CO2↑+H2O;
(2)否,改用Ba(NO3)2会使溶液中引入新的杂质离子NO3-,后面操作中无法除去;
(3)取上层清液加入BaCl2溶液,若无沉淀说明SO42-除尽;
(4)除去过量的Ba2+,减少一次过滤操作;
(5)除去溶解在溶液中的CO2及HCl;
【解析】
试题分析:(1)NH4HCO3加热易分解而除去,发生NH4HCO3 ==NH3↑+CO2↑+H2O;故答案为:除去NH4HCO3;(2)除杂时不能引入新的杂质,改用Ba(NO3)2会使溶液中引入新的杂质离子NO3-,后面操作中无法除去,故答案为:否,改用Ba(NO3)2会使溶液中引入新的杂质离子NO3-,后面操作中无法除去;(3)判断SO42-已除尽,可取上层清液加入BaCl2溶液,若无沉淀说明SO42-除尽,故答案为:取上层清液加入BaCl2溶液,若无沉淀说明SO42-除尽;(4)为避免重复操作,可先加入碳酸钠溶液,生成碳酸钡沉淀,减少实验的操作步骤,故答案为:除去过量的Ba2+,减少一次过滤操作;(5)反应后溶液中加入盐酸,生成二氧化碳气体,加热可除去溶解在溶液中的CO2及HCl,得到较为纯净的氯化钠溶液,故答案为:除去溶解在溶液中的CO2及HCl
考点:物质的分离提纯的实验方案的设计,物质分离和提纯的基本实验操作。

 N2O4,下列说法正确的是
N2O4,下列说法正确的是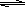 2SO3
2SO3 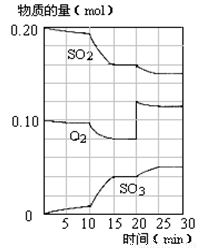
 、NO
、NO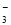 、SO
、SO
 In原子核外有49个电子
In原子核外有49个电子  Cr2O72- + 6SO42- + 14H+
Cr2O72- + 6SO42- + 14H+