题目内容
8.下列离子方程式书写正确的是( )| A. | 向苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | |
| B. | NH4HSO3溶液与足量NaOH溶液反应:HSO3-+OH-═SO32-+H2O | |
| C. | Fe(OH)2溶于稀HNO3:Fe(OH)2+2H+═Fe2++2H2O | |
| D. | 澄清石灰水与少量小苏打溶液混合:Ca2++OH-+HCO3-═CaCO3↓+H2O |
分析 A.苯酚的酸性大于碳酸氢根离子,二者反应生成的是碳酸氢根离子;
B.氢氧化钠足量,铵根离子和亚硫酸氢根离子都参与反应;
C.稀硝酸能够将亚铁离子氧化成铁离子;
D.氢氧化钙足量,反应生成碳酸钙沉淀、氢氧化钠和水.
解答 解:A.向苯酚钠溶液中通入少量CO2,反应生成苯酚和碳酸氢钠,正确的离子方程式为:C6H5O-+CO2+H2O→C6H5OH+HCO3-,故A错误;
B.NH4HSO3溶液与足量NaOH溶液混合,反应生成亚硫酸钠、一水合氨和水,正确的离子方程式为:NH4++HSO3-+2OH-=NH3•H2O+SO32-+H2O,故B错误;
C.Fe(OH)2溶于稀HNO3,二者发生氧化还原反应,正确的离子方程式为:3Fe(OH)2+NO3-+10H+═3Fe3++8H2O+NO↑,故C错误;
D.澄清石灰水与少量小苏打溶液混合,碳酸氢钠少量,反应生成碳酸钙沉淀、碳酸钠和水,反应的离子方程式为:Ca2++OH-+HCO3-═CaCO3↓+H2O,故D正确;
故选D.
点评 本题考查了离子方程式的书写判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案
相关题目
17.下列措施能提高合成氨[N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol]厂的生产效率和经济效益的是( )
①采用20MPa~50MPa的压强;
②使用催化剂;
③在合适的温度下进行反应;
④从平衡混合气体中液化分离出NH3,并将N2、H2循环使用.
①采用20MPa~50MPa的压强;
②使用催化剂;
③在合适的温度下进行反应;
④从平衡混合气体中液化分离出NH3,并将N2、H2循环使用.
| A. | ①③④ | B. | ③④ | C. | ①②③ | D. | 全部 |
18.为了证明一水合氨(NH3•H2O)是弱电解质,常温下做以下实验没有意义的是( )
| A. | 用pH试纸测出0.010mol/L氨水的pH为10 | |
| B. | 用pH试纸测定0.10mol/LNH4Cl溶液为pH<7 | |
| C. | 取出10mL0.010mol/L氨水,滴入2滴酚酞溶液,显粉红色,再加入NH4C1晶体少量,颜色变浅 | |
| D. | 取出10mL0.010mol/L氨水,滴入2滴酚酞溶液,显粉红色,再稀盐酸少量,颜色变浅 |
15.根据官能团分类,下列物质中与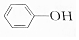 属于同一类物质的是( )
属于同一类物质的是( )
 属于同一类物质的是( )
属于同一类物质的是( )| A. | 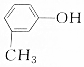 | B. | 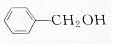 | C. | 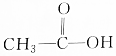 | D. | 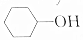 |
13.设NA表示阿伏加得德罗常数的数值,下列叙述中正确的是( )
| A. | 1 mol NH3所含有的电子数为9NA | |
| B. | 常温常压下,22.4 L氧气所含的原子数为2NA | |
| C. | 46 g NO2和N2O4的混合物含有的氮原子数为1NA | |
| D. | 物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为 NA |
20.对于0.1mol•L-1 Na2SO3溶液,正确的是( )
| A. | 升高温度,溶液的pH降低 | |
| B. | c(Na+)=2c(SO32-)+c(HSO3-)+c(H2SO3) | |
| C. | c(Na+)+c(H+)=2c(SO32-)+2c(HSO3-)+c(OH-) | |
| D. | Na2SO3溶液加热、蒸发、结晶、灼烧,所得固体的成分为Na2SO4 |
17.下列说法正确的是( )
| A. | NaCl溶于水电离出Na+和C1-,离子键发生断裂,属于化学变化 | |
| B. | 某晶体固态不导电,熔化时能导电,该晶体一定是离子晶体 | |
| C. | 干冰和水晶融化时,都克服分子间作用力 | |
| D. | PCl5、CO2、N2所有原子最外层都满足8电子结构 |
18.25℃时,pH=5的盐酸和pH=5的醋酸,以体积比1:2混合后,溶液的pH是( )
| A. | 5 | B. | 5.3 | C. | 4 | D. | 无法确定 |