��Ŀ����
9��ijʵ��С��ͬѧ�Ե绯ѧԭ��������һϵ��̽�����
��1������ͼ��Ϊijʵ��С������������ԭ��ӦFe+Cu2+=Fe2++Cu�������ӷ���ʽ��ʾ��
��Ƶ�ԭ���װ�ã���Ӧǰ���缫������ȣ�һ��ʱ������缫�������12g��������ͨ��0.2mol���ӣ�
��2�������������䣬����CuCl2��Һ��ΪNH4Cl��Һ��ʯī�缫�����ĵ缫��ӦΪ2H++2e-=H2��
����������NH4Cl��Һ�����ԣ�����ԡ��������ԡ������ԡ�����������������Ƭ��������Һ���������Թ��У������еμ��������Ʊ�����ˮ��Ȼ��μӼ���KSCN��Һ����Һ��죬�����μӹ������Ʊ�����ˮ����Һ��ɫ��ȥ��ͬѧ�ǶԴ����˶��ּ��裬ijͬѧ�ļ��裺����Һ�е�+3����������Ϊ����̬�������+3����������ΪFeO42-��д��������Ӧ�����ӷ���ʽ2Fe3++3Cl2+8H2O=2FeO42-+6Cl-+16H+
��3�������������䣬�������Ż�����ͭ������ʯī���ɵġ���װ����ͼ����ʾ��һ��ʱ����ڼ�װ��ͭ˿�����μӷ�̪��Һ����������Һ��죬�缫��ӦΪO2+2H2O+4e-=4OH-����װ����ʯī��Ϊ�������������������������������������
���� ��1��ͼ1Ϊԭ��ط�Ӧ��FeΪ������������Fe-2e-=Fe2+��ʯīΪ����������Cu2++2e-=Cu��
��2��NH4Cl����Һ��ˮ�������ԣ�������Һ�У������������ӵõ��ӣ������ӱ���������ΪFeO42-��
��3���������Ż�����ͭ������ʯī������n�ͣ���װ��Ϊ����������ʴ����Ϊ����װ�ã�
��� �⣺��1��ͼ1Ϊԭ��ط�Ӧ��FeΪ������������Fe-2e-=Fe2-��ʯīΪ����������Cu2++2e-=Cu���ܷ�ӦʽΪFe+Cu2+�TFe2++Cu��һ��ʱ������缫�������12g��
��Fe+Cu2+�TFe2++Cu �����������m ת�Ƶ���
56g 64g 56g+64g=120g 2mol
12g n
n=0.2mol��
�ʴ�Ϊ��Fe+Cu2+�TFe2++Cu��0.2��
��2�������������䣬����CuCl2��Һ��ΪNH4Cl��Һ��NH4Cl����Һ��ˮ�������ԣ�������Һ�У������������ӵõ��ӣ���ʯī�缫�����ĵ缫��ӦΪ2H++2e-=H2���������ӱ���������ΪFeO42-���䷴Ӧ�����ӷ���ʽΪ��2Fe3++3Cl2+8H2O=2FeO42-+6Cl-+16H+��
�ʴ�Ϊ��2H++2e-=H2�������ԣ�2Fe3++3Cl2+8H2O=2FeO42-+6Cl-+16H+��
��3���������Ż�����ͭ������ʯī������n�ͣ���װ��Ϊ����������ʴ����Ϊ������ͭΪ�������������� O2+2H2O+4e-�T4OH-���ʼ��ԣ��μӷ�̪����Һ��죬����װ����ͭ������ʯīΪ����������������ʯīΪ������
�ʴ�Ϊ����Һ��죻 O2+2H2O+4e-�T4OH-������
���� �����ۺϿ���ԭ��غ͵���֪ʶ�������ڵ绯ѧ֪ʶ���ۺ����õĿ��飬��Ŀ�Ѷ��еȣ�ע����յ缫��Ӧ����ʽ����д�͵����غ��ڼ����е�Ӧ��Ϊ������Ĺؼ���

 ���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д�
���Ŀ��ּ�����ҵ�����ҵ����������ϵ�д� ����ѵ��ϵ�д�
����ѵ��ϵ�д�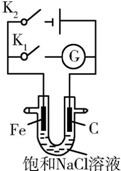
| A�� | K1�պϣ������Ϸ����ķ�ӦΪ2H++2e-�TH2�� | |
| B�� | K1�պϣ�ʯī����Χ��Һ��pH���� | |
| C�� | K2�պϣ��������ᱻ��ʴ�������������������������� | |
| D�� | K2�պϣ���·��ͨ��0.002NA������ʱ������������0.002 mol���� |
| A�� | ��״���£�22.4 L H2O���еķ�����Ϊ NA | |
| B�� | 28g N2��N4��ɵĻ�������к��е�ԭ����Ϊ2 NA | |
| C�� | 1 mol•L-1A1Cl3��Һ�к��е�Cl-��ĿΪ3 NA | |
| D�� | 2.3 g Na������ˮ��Ӧ��ת�Ƶĵ�����ĿΪ0.2 NA |
| A�� | 0.1mol•L-1��NH4��2Fe��SO4��2��Һ�У�c��NH4+��+c��NH3•H2O��+c��Fe2+��=0.3mol•L-1 | |
| B�� | �����£�pH=6��NaHSO3��Һ�У�c��SO32-��-c��H2SO3��=9.9��10-7mol•L-1 | |
| C�� | NH4HSO3��Һ�еμ�NaOH����Һǡ�ó����ԣ�c��Na+����c��SO42-��=c��NH4+����c��OH-��=c��H+�� | |
| D�� | ��Ũ�ȡ��������Na2CO3��NaHCO3��ϣ�$\frac{c��HC{{O}_{3}}^{-}��}{c��{H}_{2}C{O}_{3}��}$��$\frac{c��C{{O}_{3}}^{2-}��}{c��HC{{O}_{3}}^{-}��}$ |
| A�� | ��Ӧ�����ĵ�Zn������Ϊ97.5 g | B�� | ����A��SO2��H2�������Ϊ1��4 | ||
| C�� | ��Ӧ�б���ԭ��Ԫ��ֻ��һ�� | D�� | ��Ӧ�й�ת�Ƶ���3 mol |
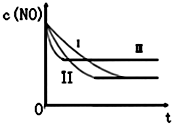 ����β���е���Ҫ��Ⱦ����NO��CO��Ϊ���������Ⱦ���������ͨ�����·�Ӧ����������β����
����β���е���Ҫ��Ⱦ����NO��CO��Ϊ���������Ⱦ���������ͨ�����·�Ӧ����������β������1����֪��2NO��g��+2CO��g��?2CO2��g��+N2��g����H=-746.5KJ/mol������Ϊʹ�ô�����
2C ��s��+O2��g��?2CO��g����H=-221.0KJ/mol
C ��s��+O2��g��?CO2��g����H=-393.5KJ/mol
��N2��g��+O2��g��=2NO��g����H=+180.5kJ•mol-1��
��2��T���£���һ�ݻ�������ܱ������У�ͨ��һ������NO��CO�������崫������ò�ͬʱ��NO��CO��Ũ�����±�
| ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
| C��NO��10-4 mol/L | 10.0 | 4.50 | C1 | 1.50 | 1.00 | 1.00 |
| C��CO��10-3 mol/L | 3.60 | 3.05 | C2 | 2.75 | 2.70 | 2.70 |
A��4.20 B��4.00 C��3.50 D��2.50
��3���о���������ʹ�õ���������ʱ����������ıȱ���������ѧ��Ӧ���ʣ������±���Ƶ�ʵ���û��������NO��Ũ����ʱ��t�仯��������ͼ��ʾ��
| ʵ�� ��� | T/��C | NO��ʼŨ ��/10-3mol•L-1 | CO��ʼŨ ��/10-3mol•L-1 | �����ı� �����/m2•g-1 |
| �� | 350 | 1.20 | 5.80 | 124 |
| �� | 280 | 1.20 | 5.80 | 124 |
| �� | 280 | 1.20 | 5.80 | 82 |
��4������ͬ���ʵ�����H2O��g����CO��g���ֱ�ͨ�����Ϊ2L�ĺ����ܱ������У����з�Ӧ��H2O��g��+CO��g��?CO2��g��+H2��g�����õ������������ݣ�
| ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ���� ��ʱ��/min | ||
| H2O | CO | CO | H2 | |||
| �� | 650 | 2 | 4 | 2.4 | 1.6 | 5 |
| �� | 900 | 1 | 2 | 1.6 | 0.4 | 3 |
| �� | 900 | a | b | c | d | t |
����a=2��b=1����c=0.6����ƽ��ʱʵ�������H2O��g����ʵ�������CO��ת���ʵĹ�ϵΪ����2 ��H2O��=��3 ��CO�������������������=������
��5��CO�����ǵĴ������ɲⶨ����β���Ƿ�����ŷű����÷����ǵĹ���ԭ��������ȼ�ϵ�أ����е�����������ƣ�Y2O3��������ﯣ�ZrO2�����壬�ܴ���O2-��
�ٸ����ĵ缫��ӦʽΪCO+2O2--2e-=CO32-��
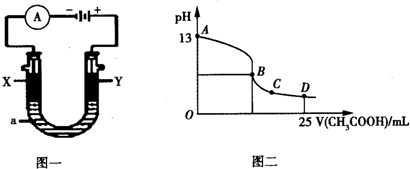
�����������Ϊ��Դ��ͨ���������ӳ�ͼһ����X��YΪʯī��aΪ2L 0.1mol/L KCl��Һ��д������ܷ�Ӧ�����ӷ���ʽ2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$Cl2��+H2��+2OH-�����һ��ʱ���ȡ25mL�����������Һ���μ�0.04mol/L����õ�ͼ�����ߣ�������������ʧ����������ˮ����Һ����仯���Բ��ƣ�������ͼ�����㣬����������������һ����̼������Ϊ2.8g��
| A�� | ��ˮ�к��зḻ�ĵ�Ԫ�أ��ʵⱻ��Ϊ������Ԫ�ء� | |
| B�� | �廯����һ����Ҫ�ĸй���ϣ�Ҳ�������˹����� | |
| C�� | ����ʢ�������ļ���ƿ��ȼ�գ�����ʲ�ɫ������ΪNaCl������ʢ�������ļ���ƿ��ȼ�գ�������ػ�ɫ������ΪFeCl3 | |
| D�� | ��ҵ�������豸��������¯�������м���ʯ��ʯ�������dz���ʯ��SiO2������ |
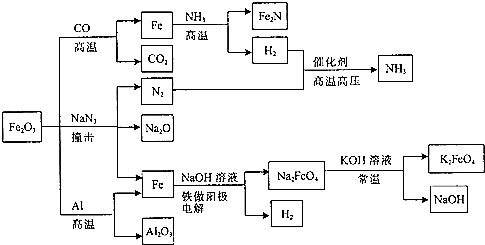
| A�� | Fe2O3��Al�ķ�Ӧ�������ȷ�Ӧ | |
| B�� | Fe2O3��NaN3��Ӧ��ÿ����1molFe2O3����9molN2 | |
| C�� | Fe2O3��CO�ķ�Ӧ�����û���Ӧ | |
| D�� | ������K2FeO4��ˮ�е��ܽ�ȱ�Na2FeO4�Ĵ� |
| �¶�/�� | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
��2����Ӧ���е�a���� 0������ڡ�����С�ڡ����ڡ�����
��3��700��ʱ��Ӧ�ٴﵽƽ�⣬Ҫʹ�ø�ƽ�������ƶ���������������ʱ�����Բ�ȡ�Ĵ�ʩ�У�����ţ���
A����С��Ӧ����� B��ͨ��CO2 C�������¶ȵ� 900��D��ʹ�ú��ʵĴ���
��4����ͼͼ����Ϸ�Ӧ�ٵ��ǣ�����ţ���ͼ�Ц��ǻ������CO�ĺ�����TΪ�¶ȣ���
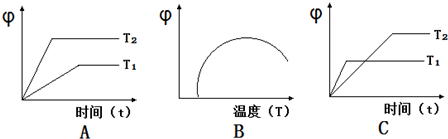
��5����Ӧ��2Fe��s��+O2��g���T2FeO��s����H3=2��a+b��kJ•mol-1��