题目内容
下列叙述正确的是( )
| A、常温时,某溶液中由水电离出来的c(H+ )和c(OH- )的乘积为1×10-24,该溶液中一定可以大量存在K+、Na+、AlO2-、SO4 2- | ||
B、常温时,0.1mol/L HA溶液的pH>1,0.1mol/L BOH溶液中
| ||
| C、油脂、淀粉和蛋白质在一定条件下都能发生水解反应 | ||
| D、SiO2和Al2O3都既能与酸反应,又能与碱反应,二者都属于两性氧化物 |
考点:离子浓度大小的比较,离子共存问题,两性氧化物和两性氢氧化物,油脂的性质、组成与结构
专题:
分析:A.由水电离出来的c(H+ )和c(OH- )的乘积为1×10-24,为酸或碱溶液;
B.0.1mol/L HA溶液的pH>1,HA为弱酸,0.1mol/L BOH溶液中
=1012,BOH为强碱,两种溶液等体积混合恰好生成BA,A-水解显碱性;
C.油脂中含-COOC-,淀粉为多糖,蛋白质中含-CONH-,均可水解;
D.SiO2为酸性氧化物.
B.0.1mol/L HA溶液的pH>1,HA为弱酸,0.1mol/L BOH溶液中
| c(OH-) |
| c(H+) |
C.油脂中含-COOC-,淀粉为多糖,蛋白质中含-CONH-,均可水解;
D.SiO2为酸性氧化物.
解答:
解:A.由水电离出来的c(H+ )和c(OH- )的乘积为1×10-24,为酸或碱溶液,酸溶液中H+、AlO2-结合生成沉淀,不能共存,故A不选;
B.0.1mol/L HA溶液的pH>1,HA为弱酸,0.1mol/L BOH溶液中
=1012,BOH为强碱,两种溶液等体积混合恰好生成BA,A-水解显碱性,则c(OH- )>c(H+ ),水解程度较小,则c(B+ )>c(A-)>c(OH- )>c(H+ ),故B错误;
C.油脂中含-COOC-,水解生成高级脂肪酸(或盐)和甘油;淀粉为多糖,水解最终产物为葡萄糖;蛋白质中含-CONH-,水解生成氨基酸,故C正确;
D.SiO2为酸性氧化物,Al2O3既能与酸反应,又能与碱反应生成盐和水,则属于两性氧化物,故D错误;
故选C.
B.0.1mol/L HA溶液的pH>1,HA为弱酸,0.1mol/L BOH溶液中
| c(OH-) |
| c(H+) |
C.油脂中含-COOC-,水解生成高级脂肪酸(或盐)和甘油;淀粉为多糖,水解最终产物为葡萄糖;蛋白质中含-CONH-,水解生成氨基酸,故C正确;
D.SiO2为酸性氧化物,Al2O3既能与酸反应,又能与碱反应生成盐和水,则属于两性氧化物,故D错误;
故选C.
点评:本题考查较综合,涉及离子浓度大小的比较、离子的共存、有机物的结构与性质、两性氧化物的判断等,为高考中常见的冷拼凑试题,注重高频考点的考查,题目难度不大.

练习册系列答案
相关题目
下列说法,不正确的是( )
| A、Na2O2可用于呼吸面具中氧气的来源 |
| B、Na2O和Na2O2投入水中都能生成NaOH,都是氧化还原反应,它们都是碱性氧化物 |
| C、Na2CO3可用于制玻璃、肥皂、造纸、纺织等工业,而NaHCO3可用于治胃酸过多,制发酵粉等 |
| D、NaCl的性质稳定,可用作调味品 |
 5℃时,在20mL的盐酸中,逐滴加入0.2mol?L-1的氨水,溶液的pH与氨水体积关系如图所示,则下列说法不正确的是( )
5℃时,在20mL的盐酸中,逐滴加入0.2mol?L-1的氨水,溶液的pH与氨水体积关系如图所示,则下列说法不正确的是( )| A、B点的横坐标a>10 |
| B、滴加前盐酸的物质的量浓度为0.1mol?L-1 |
| C、A、B间的任一点,溶液都有c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| D、如果将氨水换为NaOH溶液,则滴加20mL时溶液的pH一定大于C点的pH |
钡和钠相似,也能形成O22-离子的过氧化物,下列叙述中正确的是( )
| A、过氧化钡的化学式为Ba2O2 |
| B、晶体中阴阳离子个数比为2:1 |
| C、1mol过氧化钡与足量水反应生成0.5mol氧气 |
| D、过氧化钠和过氧化钡都是强氧化剂 |
下列各组离子一定能大量共存的是( )
| A、滴加石蕊试液显红色的溶液:Fe3+、NH4+、C1-、SCN- |
| B、含有大量HCO3-的溶液:NH4+、Ca2+、Mg2+、I- |
| C、在加入铝粉能产生H2的溶液中:NH4+、Fe2+、SO42-、NO3- |
| D、含有大量ClO-的溶液:OH-、K+、I-、SO32- |
设NA为阿伏加德罗常数,下列说法不正确的是( )
| A、标况下,NA个甲烷和22.4L甲烷的质量相等 |
| B、1molNa2O2固体中含有离子总数为3NA个 |
| C、23 g金属钠变为钠离子时得到的电子数为NA |
| D、标况下,44.8L氦气所含的原子数目为2NA |
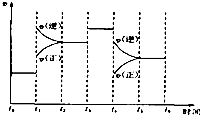 已知2A2(g)+B2(g)?2C3(g);△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2mol A2和1mol B2,在500℃时充分反应达平衡后C3的浓度为w mol/L,放出热量b kJ.
已知2A2(g)+B2(g)?2C3(g);△H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2mol A2和1mol B2,在500℃时充分反应达平衡后C3的浓度为w mol/L,放出热量b kJ.