题目内容
11. 如图是研究部分元素氢化物的沸点变化规律的图象,折线c可以表达出第ⅣA族元素氢化物的沸点变化规律.两位同学对某主族元素氢化物的沸点的变化趋势画出了两条折线--折线a和折线b,你认为正确的是b(填“a”或“b”),理由是A点所示的氢化物是水,其沸点高是由于水分子间存在氢键,所以氧族元素中其他氢化物的沸点不会高于水.
如图是研究部分元素氢化物的沸点变化规律的图象,折线c可以表达出第ⅣA族元素氢化物的沸点变化规律.两位同学对某主族元素氢化物的沸点的变化趋势画出了两条折线--折线a和折线b,你认为正确的是b(填“a”或“b”),理由是A点所示的氢化物是水,其沸点高是由于水分子间存在氢键,所以氧族元素中其他氢化物的沸点不会高于水.
分析 线c逐渐上升,表明没有氢键的影响,是第ⅣA族元素氢化物的沸点变化规律;A点所示的氢化物是水,其沸点高是由于水分子间存在氢键.
解答 解:线c逐渐上升,表明没有氢键的影响,是第ⅣA族元素氢化物的沸点变化规律.A点所示的氢化物是水,其沸点高是由于水分子间存在氢键,所以氧族元素中其他氢化物的沸点不会高于水,故b正确,
故答案为:ⅣA;b;A点所示的氢化物是水,其沸点高是由于水分子间存在氢键,所以氧族元素中其他氢化物的沸点不会高于水.
点评 本题考查元素周期律、分子结构与性质、氢键,涉及氢键对物质性质的影响等,难度不大,注意分析图象中所给的信息,侧重于考查学生的分析能力.

练习册系列答案
 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案
相关题目
1.把a、b、c、d 4块金属浸入稀硫酸中,用导线两两相连组成原电池.若把a、b相连时,a为负极;若a、c相连时,电流由c经导线流向a; b、d相连时,电子经由导线由d流向b,则四种金属的活动顺序由强到弱的顺序是( )
| A. | a>b>c>d | B. | a>c>d>b | C. | c>a>b>d | D. | b>a>c>d |
19.下列结论错误的是 ( )
①微粒半径:K+>Al3+>S2->Cl-
②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③离子的还原性:S2->Cl->Br->I-
④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO4
⑥非金属性:O>N>P>Si
⑦金属性:Be<Mg<Ca<K.
①微粒半径:K+>Al3+>S2->Cl-
②氢化物的稳定性:HF>HCl>H2S>PH3>SiH4
③离子的还原性:S2->Cl->Br->I-
④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO4
⑥非金属性:O>N>P>Si
⑦金属性:Be<Mg<Ca<K.
| A. | 只有① | B. | ①③⑤ | C. | ②④⑤⑥⑦ | D. | ②④⑥ |
6.下列关于能层与能级的说法中正确的是( )
| A. | 原子核外每一个能层最多可容纳的电子数为n2 | |
| B. | 任一能层的能级总是从s能级开始,而且能级数等于该能层数 | |
| C. | 不同能层中s电子的原子轨道半径相同 | |
| D. | 不同能层中p电子的原子轨道能量相同 |
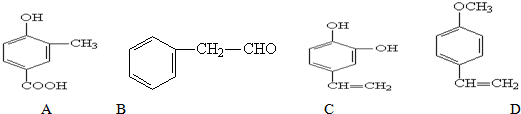
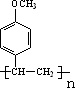
16.某有机物的结构简式为 ,它在一定条件下可能发生的反应有( )
,它在一定条件下可能发生的反应有( )
①加成 ②水解 ③酯化 ④氧化 ⑤消去.
 ,它在一定条件下可能发生的反应有( )
,它在一定条件下可能发生的反应有( )①加成 ②水解 ③酯化 ④氧化 ⑤消去.
| A. | ①③④ | B. | ①③④⑤ | C. | ②③④ | D. | ①③⑤ |
20.某化合物由A,B 2种元素组成,已知A,B两元素的质量比为7:4,相对原子质量之比为7:8,则此化合物分子式可能是( )
| A. | A2B | B. | AB | C. | AB2 | D. | A2B4 |
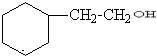 .
. .
.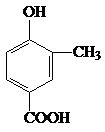 +CH3CH2OH$?_{△}^{浓硫酸}$
+CH3CH2OH$?_{△}^{浓硫酸}$ +H2O.
+H2O.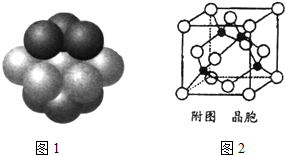 铁和铜都是日常生活中常见的金属,有着广泛的用途.请回答下列问题:
铁和铜都是日常生活中常见的金属,有着广泛的用途.请回答下列问题: