题目内容
2.某白色粉末由两种物质组成,为鉴别其成分进行如下实验:①取少量样品加入足量水仍有部分固体未溶解;继续加入足量稀盐酸,有气泡产生,固体全部溶解;
②取少量样品加入足量稀硫酸有气泡产生,振荡后仍有固体存在.
该白色粉末可能为( )
| A. | Na2CO3、Al(OH)3 | B. | AgCl、NaHCO3 | C. | NaHCO3、BaCO3 | D. | Na2SiO3、CuO |
分析 ①取少量样品加入足量水仍有部分固体未溶解,说明有一种物质不溶于水,再加入足量稀盐酸,有气泡产生,固体全部溶解,则至少有一种物质可与盐酸反应生成气体,可能为二氧化碳或二氧化硫;
②取少量样品加入足量稀硫酸有气泡产生,震荡后仍有固体存在,说明在振荡过程中生成不溶于酸的固体,以此解答该题.
解答 解:A.Na2CO3、Al(OH)3都与盐酸反应,硫酸足量时没有固体剩余,故A错误;
B.碳酸氢钠与盐酸反应生成气体,AgCl不溶于盐酸,故B错误;
C.BaCO3不溶于水,二者都与盐酸反应,且生成气体,若加入足量稀硫酸,有气泡产生,且BaCO3,能和H2SO4反应生成BaSO4沉淀,故C正确;
D.加入盐酸,没有气泡生成,且生成硅酸沉淀,故D错误.
故选C.
点评 本题考查物质的检验和鉴别,侧重于元素化合物知识的综合理解和运用的考查,注意把握物质的性质,为解答该题的关键,难度中等.

练习册系列答案
相关题目
13.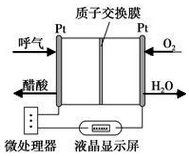 查司机酒驾的一种酸性染料电池酒精检测仪示意如图,它适合现场吹气酒精检测.下列说法不正确的是( )
查司机酒驾的一种酸性染料电池酒精检测仪示意如图,它适合现场吹气酒精检测.下列说法不正确的是( )
 查司机酒驾的一种酸性染料电池酒精检测仪示意如图,它适合现场吹气酒精检测.下列说法不正确的是( )
查司机酒驾的一种酸性染料电池酒精检测仪示意如图,它适合现场吹气酒精检测.下列说法不正确的是( )| A. | 电流由呼气所在的铂电极流出 | |
| B. | O2所在的铂电极处发生还原反应 | |
| C. | 该电池工作一段时间后,正极区pH减小 | |
| D. | 该电池的负极反应式为:CH3CH2OH-4e-+H2O=CH3COOH+4H+ |
10.已知酸性:H2SO3>H2S,下列实验操作后的反应液内肯定没有不溶物的是( )
| A. | 将SO2气体通入足量澄清石灰水 | |
| B. | 在Na2S溶液中通入SO2气体直至过过量 | |
| C. | 在Na2SO3溶液中通入H2S气体直至过量 | |
| D. | 将8.7克MnO2固体与含0.4mol溶质的浓盐酸加热并充分反应后 |
17.在通常条件下,下列各组物质的性质排列正确的是( )
| A. | 熔点:CO2>KCl>SiO2 | B. | 水溶性:HCl>H2S>SO2 | ||
| C. | 沸点:NaH>H2O>H2S | D. | 硬度:SiC>石墨>CaCO3 |
14.为提纯下列物质(括号内为杂质),选用的试剂和分离方法都正确的是( )
| 选项 | 物质 | 试剂 | 分离方法 |
| A | 乙酸乙酯(乙酸) | 氢氧化钠溶液 | 分液 |
| B | 苯(苯酚) | 饱和溴水 | 过滤 |
| C | 乙烷(乙烯) | 溴水 | 洗气 |
| D | 乙烯(二氧化硫) | 酸性高锰酸钾溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
11.合金由于其众多的优点而被航空、航天、航海业广泛关注.下列不属于铝锂合金优点的是( )
| A. | 密度大 | B. | 硬度大 | C. | 抗腐蚀 | D. | 高强度 |
12.氯气是一种化学性质很活泼的非金属单质,它具有较强的氧化性,下列叙述中不正确的是( )
| A. | 铁在氯气中燃烧,生成棕红色的烟 | |
| B. | 红热的铜丝在氯气里剧烈燃烧,生成棕黄色的烟 | |
| C. | 纯净的H2在Cl2中安静地燃烧,发出苍白色火焰,集气瓶口呈现白色烟雾 | |
| D. | 氯气能与水反应生成次氯酸和盐酸,久置氯水最终变为稀盐酸 |
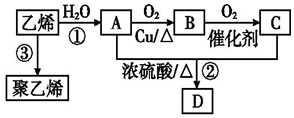
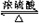 CH3COOC2H5+H2O; 反应类型:酯化反应.
CH3COOC2H5+H2O; 反应类型:酯化反应. ; 反应类型:加聚反应.
; 反应类型:加聚反应.