��Ŀ����
(6��)A��B���ֶ�����Ԫ�أ�A�������������Ǵ�����������������B������������������ڲ����������һ�룬B�ĵ�����A�ĵ�����ȼ�գ������������ֹ�̬�����1.55 g��B������1.6 gA������ȼ�գ�����Ӧ��ľ������ų�X kJ������
��1��ͨ������ȷ���������ɣ��û�ѧʽ��ʾ���� ������Ӧ��������g��Ϊ ��
��2����֪B���ʵ�ȼ����ΪY kJ/mol����B�ĵ�����A�ĵ�����ȼ�����ɵͼ�̬��������Ȼ�ѧ����ʽΪ ��
��1�� P2O3��P2O5 �� 1.375g��1.775g ������1�֣�ǰ���Ӧ��
![]() ��2�� P(s)��
��2�� P(s)��![]() O2(g)=
O2(g)=![]() P2O3(s)����H����(40X��Y)kJ/mol ������ƽ����Ӧ�ȸ�1�֣�
P2O3(s)����H����(40X��Y)kJ/mol ������ƽ����Ӧ�ȸ�1�֣�

��ϰ��ϵ�д�
�����Ŀ
 ������E������������Ӧˮ���ﷴӦ�Ļ�ѧ����ʽ�� ��
������E������������Ӧˮ���ﷴӦ�Ļ�ѧ����ʽ�� �� �ϵ�أ��˵�صĸ�����Ӧʽ�� ��
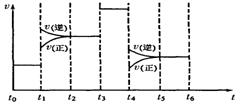
�ϵ�أ��˵�صĸ�����Ӧʽ�� �� 2CA3(g)������Ӧ�ﵽƽ��ʱ���ϸı�����(���ı�A2��C2��CA3����)����ͼ��ʾ��Ӧ�����뷴Ӧ���̵Ĺ�ϵ�����б�ʾƽ��������CA3�ĺ�����ߵ�һ��ʱ����
���¶�ΪT��ʱ����4amolA2��2a molC2����1L�ܱ������У���ַ�Ӧ����C2��ת����Ϊ50������ƽ��������C2���������Ϊ ��ƽ��ʱѹǿΪ��ʼѹǿ�� ����
2CA3(g)������Ӧ�ﵽƽ��ʱ���ϸı�����(���ı�A2��C2��CA3����)����ͼ��ʾ��Ӧ�����뷴Ӧ���̵Ĺ�ϵ�����б�ʾƽ��������CA3�ĺ�����ߵ�һ��ʱ����
���¶�ΪT��ʱ����4amolA2��2a molC2����1L�ܱ������У���ַ�Ӧ����C2��ת����Ϊ50������ƽ��������C2���������Ϊ ��ƽ��ʱѹǿΪ��ʼѹǿ�� ����