题目内容
已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3kJ/mol,则下列说法正确的是( )
| A、浓硫酸和稀NaOH溶液反应,生成 l mol水时放热57.3 kJ |
| B、含l molH2SO4的稀硫酸与足量稀NaOH溶液中和后,放热为57.3 kJ |
| C、1L 0.l mol/L CH3COOH与1L 0.l1 mol/L NaOH溶液反应后放热为5.73 kJ |
| D、1L 0.l mol/L HNO3与1L 0.l1 mol/L NaOH溶液反应后放热为5.73 kJ |
考点:有关反应热的计算
专题:
分析:A、浓硫酸稀释放出大量的热;
B、NaOH足量,1mol H2SO4的稀硫酸与2molNaOH溶液中和生成2mol水;
C、醋酸是弱电解质,电离需吸收热量;
D、硝酸为强酸,氢氧化钠为强碱,二者的稀溶液反应生成0.1molH2O后放热为5.73 kJ.
B、NaOH足量,1mol H2SO4的稀硫酸与2molNaOH溶液中和生成2mol水;
C、醋酸是弱电解质,电离需吸收热量;
D、硝酸为强酸,氢氧化钠为强碱,二者的稀溶液反应生成0.1molH2O后放热为5.73 kJ.
解答:
解:A、浓硫酸稀释放出大量的热,浓硫酸与稀NaOH溶液完全反应生成1mol水时放出的热量包括中和热和溶解热,故大于57.3 kJ,故A错误;
B、NaOH足量,1mol H2SO4的稀硫酸与2molNaOH溶液中和后,放热为114.6kJ,故B错误;
C、醋酸是弱电解质,电离需吸收热量,稀醋酸与稀NaOH溶液反应生成1mol水,放出的热量小于57.3 kJ,故C错误;
D、硝酸为强酸,氢氧化钠为强碱,1L0.1 mol/L HNO3与1L 0.1mol/L NaOH溶液反应后放热为5.73 kJ,故D正确;
故选D.
B、NaOH足量,1mol H2SO4的稀硫酸与2molNaOH溶液中和后,放热为114.6kJ,故B错误;
C、醋酸是弱电解质,电离需吸收热量,稀醋酸与稀NaOH溶液反应生成1mol水,放出的热量小于57.3 kJ,故C错误;
D、硝酸为强酸,氢氧化钠为强碱,1L0.1 mol/L HNO3与1L 0.1mol/L NaOH溶液反应后放热为5.73 kJ,故D正确;
故选D.
点评:本题考查学生对于反应热、中和热的理解及有关计算等,难度不大,注意强酸、强碱的稀溶液中和热为57.3kJ/mol.

练习册系列答案
相关题目
将足量BaCO3(Ksp=8.1×10-9) 分别加入:①30mL 水; ②10mL 0.2mol/LNa2CO3溶液; ③50mL 0.01mol/L 氯化钡溶液; ④100mL 0.01mol/L盐酸中溶解至溶液饱和.
请确定各溶液中Ba2+的浓度由大到小的顺序为( )
请确定各溶液中Ba2+的浓度由大到小的顺序为( )
| A、①②③④ | B、③④①② |
| C、④③①② | D、②①④③ |
立方烷(C8H8)的碳架结构如图,则它的五氯代物有( )种
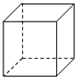

| A、3 | B、4 | C、5 | D、6 |
工业上可用铝槽储装浓硝酸,其原因是( )
| A、浓硝酸是弱酸 |
| B、浓硝酸的氧化性比较弱 |
| C、铝表面可被氧化生成一层致密的保护膜 |
| D、铝的化学性质不活泼 |
下表为4种常见溶液中溶质的质量分数和物质的量浓度:这4种溶液中密度最小的是( )
| 溶 质 | HCl | NaOH | CH3COOH | HNO3 |
| 溶质的质量分数/% | 36.5 | 40 | 60 | 63 |
| 物质的量浓度/mol L-1 | 11.8 | 14.3 | 10.6 | 13.8 |
| A、HCl |
| B、NaOH |
| C、CH3COOH |
| D、NO3 |
在2L溶有0.2mol NaCl和0.2mol MgCl2的溶液中,Cl-的物质的量浓度为( )
| A、0.05 mol/L |
| B、0.1 mol/L |
| C、0.2mol/L |
| D、0.3 mol/L |
0.2molNa218O2与足量CO2完全反应后,所得固体质量为( )
| A、21.2g |
| B、21.6g |
| C、22.0g |
| D、22.4g |
下列说法中错误的是( )
| A、1gO2与1gO3所含的原子数目相等 |
| B、不同分散系其对应分散质的微粒直径不同 |
| C、标况下1molCCl4所占体积约为22.4L |
| D、NaCl晶体和熔化的NaCl都属于电解质 |