题目内容
11.下列关于乙烯的说法正确的是( )| A. | 是天然气的主要成分 | B. | 不能使稀的酸性高锰酸钾溶液褪色 | ||
| C. | 是一种植物生长调节剂 | D. | 是聚乙烯塑料袋的主要成分 |
分析 A、天然气的主要成分是甲烷;
B、乙烯中的碳碳双键能被高锰酸钾溶液氧化;
C、乙烯是植物激素;
D、乙烯加聚得聚乙烯.
解答 解:A、天然气的主要成分是甲烷,而不是乙烯,故A错误;
B、乙烯中的碳碳双键能被高锰酸钾溶液氧化,即高锰酸钾能被乙烯还原而褪色,故B错误;
C、乙烯是植物激素,故能调节植物的生长和成熟,故C正确;
D、乙烯加聚得聚乙烯,故聚乙烯塑料袋的成分是聚乙烯,乙烯只是生产聚乙烯的原料,故D错误.
故选C.
点评 本题考查了乙烯的性质和用途,难度不大,应注意的是乙烯能使高锰酸钾溶液褪色和能使溴水褪色的原因不同.

练习册系列答案
相关题目
2.下列实验或操作正确的是( )
| A. | 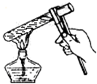 加热试管中的液体 | B. | 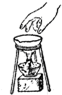 移走蒸发皿 | ||
| C. | 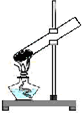 加热结晶水合物 | D. | 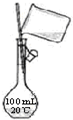 向容量瓶中转移溶液 |
19.CO2是一种温室气体.CO2属于( )
| A. | 酸 | B. | 碱 | C. | 有机物 | D. | 酸性氧化物 |
6.某澄清溶液中存在大量的Ba2+、NH4+、Cl-,该溶液中还可能大量存在的离子是( )
| A. | Fe3+ | B. | CO32- | C. | Ag+ | D. | OH- |
1.下列说法不正确的是( )
| A. | 用分液漏斗分液时,先打开旋塞,待下层液体完全分出后,关闭旋塞,再从上口倒出上层液体 | |
| B. | 在油脂皂化反应实验中,用玻璃棒蘸取反应液滴入热水中,若无油滴浮于液面上,说明皂化反应已经完全 | |
| C. | 在中和热测定实验中,盐酸和NaOH溶液的总质量m g,反应前后体系温度变化△t℃,反应液的比热容为c J•g-1•℃-1,则生成1mol水放出的热量为cm△t×10-3kJ | |
| D. | 同一温度下,可通过观察出现浑浊的快慢来探究浓度对Na2S2O3与稀硫酸反应速率的影响 |