题目内容
现向一容积不变的2L密闭容器中充入4mol NH3和3mol O2,发生反应4NH3(g)+3O2(g)?2N2(g)+6H2O(g),4min后,测得生成的H2O占混合气体体积的40%,则下列表示此段时间内该反应的平均速率不正确的是( )
| A、v(N2)=0.125 mol?L-1?min-1 |
| B、v(H2O)=0.375 mol?L-1?min-1 |
| C、v(O2)=0.225 mol?L-1?min-1 |
| D、v(NH3)=0.250 mol?L-1?min-1 |
考点:反应速率的定量表示方法
专题:化学反应速率专题
分析:先根据三段式求出物质的物质的量,然后根据v=
=
来解答.
| △c |
| △t |
| △c |
| V?△t |
解答:
解:设反应的NH3为4xmol,
4NH3(g)+3O2(g)?2N2(g)+6H2O(g),
起始(mol) 4 3 0 0
反应量(mol) 4x 3x 2x 6x
平衡量(mol) 4-4x 3-3x 2x 6x
4min后,测得生成的H2O占混合气体体积的40%,则有
×100%=40%,解得x=0.5;
A、v(N2)=
=0.125mol?L-1?min-1,故A正确;
B、v(H2O)=
=0.375mol?L-1?min-1,故B正确;
C、v(O2)=
=0.1875mol?L-1?min-1,故C错误;
D、v(NH3)=
=0.250mol?L-1?min-1,故D正确;
故选C.
4NH3(g)+3O2(g)?2N2(g)+6H2O(g),
起始(mol) 4 3 0 0
反应量(mol) 4x 3x 2x 6x
平衡量(mol) 4-4x 3-3x 2x 6x
4min后,测得生成的H2O占混合气体体积的40%,则有
| 6x |
| 7+x |
A、v(N2)=
| 1mol |
| 2L×4min |
B、v(H2O)=
| 3mol |
| 2L×4min |
C、v(O2)=
| 1.5mol |
| 2L×4min |
D、v(NH3)=
| 2mol |
| 2L×4min |
故选C.
点评:本题主要考查了三段法计算以及化学反应速率的计算,难度不大,注意基础公式的应用.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
下列物质中互为同分异构体的是( )
| A、甲烷和乙烷 |
| B、二氧化碳和干冰 |
| C、石墨和金刚石 |
| D、正丁烷和异丁烷 |
下列叙述正确的是( )
| A、同种元素的原子均具有相同的质子数和中子数 |
| B、不同元素的原子构成的分子只含极性键 |
| C、第三周期中的非金属元素的气态氢化物还原性越强,对应元素的最高价含氧酸酸性越弱 |
| D、第ⅠA族和第ⅦA族元素从上到下随原子序数递增,单质的沸点均逐渐升高 |
下列四种粒子的结构示意图中,属于稀有气体元素的原子是( )
A、 |
B、 |
C、 |
D、 |
下列有关化学用语表示正确的是( )
| A、乙炔的电子式H:C:::C:H |
B、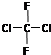 和 和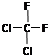 是同一物质 是同一物质 |
C、对甲基苯甲醇的结构简式: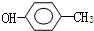 |
D、乙醇分子的比例模型: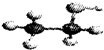 |
以“物质的量”为中心的计算是化学计算的基础,下列与“物质的量”相关的计算正确的( )
| A、现有CO、CO2、O3三种气体,它们分别都含有1molO,则三种气体的物质的量之比为 3:2:1 |
| B、5.6g CO 和22.4L CO2中含有的碳原子数一定相等 |
| C、标准状况下,11.2 L X气体分子的质量为16 g,则X气体的摩尔质量是32 |
| D、n g Cl2中有m个Cl原子,则阿伏加德罗常数NA的数值可表示为 35.5m/n |
下列关于浓硫酸和稀硫酸的叙述中正确的是( )
| A、都能作干燥剂 |
| B、加热时都能与铜发生反应 |
| C、都具有一定的氧化性 |
| D、在常温下都能用铁制容器贮存 |
