题目内容
一定条件下,在四个恒定密闭容器中分别进行下列反应,其中依据“容器内气体压强不变”可判定该反应达到平衡状态的是( )
| A、CO2(g)+H2(g)?CO(g)+H2O(g) |
| B、C(s)+CO2(g)?2CO(g) |
| C、2HI(g)?H2(g)+I2(g) |
| D、FeO(s)+CO(g)?Fe(s)+CO2(g) |
考点:化学平衡状态的判断
专题:化学平衡专题
分析:依据“容器内气体压强不变”可判定该反应达到平衡状态的反应是前后气体系数和变化的反应.
解答:
解:依据“容器内气体压强不变”可判定该反应达到平衡状态的反应是前后气体系数和变化的反应;
A、反应是前后气体系数和不变化的反应,故A错误;
B、反应是前后气体系数和变化的反应,故B正确;
C、反应是前后气体系数和不变化的反应,故C错误;
D、反应是前后气体系数和不变化的反应,故D错误;
故选B.
A、反应是前后气体系数和不变化的反应,故A错误;
B、反应是前后气体系数和变化的反应,故B正确;
C、反应是前后气体系数和不变化的反应,故C错误;
D、反应是前后气体系数和不变化的反应,故D错误;
故选B.
点评:本题通过压强是否变化来确定反应是否达到了平衡,反应前后气体系数和相等的反应,当压强不变的状态不一定是平衡状态.

练习册系列答案
相关题目
下列反应的离子方程式书写不正确的是( )
| A、向KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液至SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O |
| B、碳酸氢钠溶液与少量硫酸氢钠溶液反应:HCO3-+H+=CO2↑+H2O |
| C、少量稀硫酸溶液加入氢氧化钡溶液中:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
| D、硫酸铝与足量氨水反应:Al3++3 NH3?H2O=Al(OH)3↓+3NH4+ |
下列事实能用勒夏特列原理解释的是( )
| A、H2、I2、HI平衡混合气体加压后颜色变深 |
| B、使用催化剂,提高合成氨的产率 |
| C、高锰酸钾(KMnO4)溶液加水稀释后颜色变浅 |
| D、新制的氯水在光照条件下颜色变浅 |
有机物分子中的原子(团)之间会相互影响,导致相同的原子(团)表现不同的性质.下列各项的事实不能说明上述观点的是( )
| A、甲苯能使酸性高锰酸钾溶液褪色,而甲基环己烷不能使酸性高锰酸钾褪色 |
| B、乙烯能与溴水发生加成反应,而乙烷不能发生加成反应 |
| C、苯酚与溴水可直接反应,而苯与液溴反应则需要铁作催化剂 |
| D、苯与硝酸在加热时发生取代反应,甲苯与硝酸在常温下就能发生取代反应 |
金属铜与人体分泌物中的盐酸以及体内的空气反应可生成超氧酸:Cu+HCl+O2=CuCl+HO2,HO2 (超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性.下列说法或表示错误的是( )
| A、氧化剂是O2 |
| B、HO2在碱中不能稳定存在 |
| C、氧化产物是HO2 |
| D、1mol Cu参加反应有1mol电子发生转移 |
下列判断不合理的是( )
| A、能电离出H+的物质不一定是酸 |
| B、蔗糖、碳酸钡和水分别属于非电解质、强电解质和弱电解质 |
| C、根据分散系中分散质粒子直径大小将分散系分为溶液、胶体和浊液 |
| D、焰色反应是化学变化 |
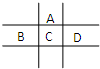 有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的单质可与酸反应,1mol E单质与足量酸作用,在标准状况下能产生33.6L H2;E的阳离子与A的阴离子核外电子层结构完全相同,回答下列问题:
有A、B、C、D、E五种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示.E的单质可与酸反应,1mol E单质与足量酸作用,在标准状况下能产生33.6L H2;E的阳离子与A的阴离子核外电子层结构完全相同,回答下列问题: