题目内容
NA为阿伏加德罗常数,下列说法正确的是( )
| A、0.5mol?L-1Na2SO4溶液中所含的Na+数为NA |
| B、常温常压下,4g氦气所含有的质子数为4NA |
| C、1molCl2与足量Fe反应,转移的电子数为3NA |
| D、标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g |
考点:阿伏加德罗常数
专题:
分析:A.缺少硫酸钠溶液的体积,无法计算钠离子的物质的量及数目;
B.氦气为单原子分子,4g氦气含有1mol氦气,含有2mol质子;
C.1mol氯气完全反应最多得到2mol电子;
D.CO、乙烯的摩尔质量都是28g/mol,分子数为NA的气体的物质的量为1mol,标况下气体体积约为22.4L.
B.氦气为单原子分子,4g氦气含有1mol氦气,含有2mol质子;
C.1mol氯气完全反应最多得到2mol电子;
D.CO、乙烯的摩尔质量都是28g/mol,分子数为NA的气体的物质的量为1mol,标况下气体体积约为22.4L.
解答:
解:A.没有告诉0.5mol?L-1Na2SO4溶液的体积,无法计算溶液中钠离子的数目,故A错误;
B.4g氦气的物质的量为1mol,1mol氦气中含有1mol氦原子,含有2mol质子,含有的质子数为2A,故B错误;
C.1mol氯气与铁完全反应得到2mol电子,转移的电子数为2NA,故C错误;
D.标准状况下,分子数为NA的CO、C2H4混合气体的物质的量为1mol,标况下1mol混合气体的体积约为22.4 L,质量约为28g,故D正确;
故选D.
B.4g氦气的物质的量为1mol,1mol氦气中含有1mol氦原子,含有2mol质子,含有的质子数为2A,故B错误;
C.1mol氯气与铁完全反应得到2mol电子,转移的电子数为2NA,故C错误;
D.标准状况下,分子数为NA的CO、C2H4混合气体的物质的量为1mol,标况下1mol混合气体的体积约为22.4 L,质量约为28g,故D正确;
故选D.
点评:本题考查阿伏加德罗常数的综合应用,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项B注意稀有气体为单原子分子,试题利于提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
下列溶液中c(Cl-)与50mL 1mol/L AlCl3溶液中c(Cl-)相等是( )
| A、100mL 3mol/L KCl溶液 |
| B、25mL 2mol/L AlCl3溶液 |
| C、150mL 1mol/L NaCl溶液 |
| D、25mL 1.5mol/L MgCl2溶液 |
分别取1g左右某脂肪酸(M<300):①与含I2为2.7g的碘的CCl4溶液完全加成;②与含0.2gKOH的溶液所中和.由此推测该脂肪酸的准确相对分子质量可能为( )
| A、290 | B、282 |
| C、280 | D、278 |
下列说法正确的是( )
| A、互为同位素的原子性质几乎完全相同 |
| B、丙氨酸CH3-CH(NH2)-COOH存在手性异构体 |
| C、标准状况下,相同体积的NH3、CH4、HF含有相同的电子数 |
| D、等体积的NO和O2混合后所得的混合气体的平均摩尔质量为41.33 g/mol |
下列离子方程式书写正确的是( )
| A、赤铁矿投入到稀盐酸中:FeO+2H+═Fe2++H2O |
| B、FeCl3溶液中加入氢氧化钠溶液:Fe2++3OH-═Fe(OH)2↓ |
| C、三氯化铁溶液中加入铁粉:2Fe3++Fe═3Fe2+ |
| D、FeCl2溶液跟Cl2反应:Fe2++Cl2═Fe3++2Cl- |
绿色化学的核心是反应过程的绿色化,即要求原料物质中的所有原子完全被利用且全部转入期望的产品中,下列过程不符合这一思想的是( )
A、甲烷与氯气反应制氯仿:CH4+3Cl2
| ||
B、烯烃与水煤气发生的羰基合成反应:RCH=CH2+CO+H2
| ||
C、甲烷、CO合成乙酸乙酯:2CH4+2CO
| ||
D、乙烯合成聚乙烯nCH4+2CO
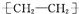 |
乘车前都要进行安检,易燃、易爆、剧毒、易腐蚀、强氧化剂等物品严禁上车.下列物品可让乘客带上车的是( )
①浓硫酸 ②氰化钾 ③水银 ④汽油 ⑤黑火药 ⑥白磷 ⑦酒精.
①浓硫酸 ②氰化钾 ③水银 ④汽油 ⑤黑火药 ⑥白磷 ⑦酒精.
| A、①④⑤ |
| B、①②⑥⑦ |
| C、①③④⑤⑦ |
| D、全部都不能带上车 |