题目内容
7.(1)甲同学在用FeSO4固体配制FeSO4溶液时,除了加入蒸馏水外,还需加Fe和H2SO4试剂(填化学式)(2)乙同学为标定某醋酸溶液的准确浓度,用0.2000mol•L-1的NaOH溶液对20.00mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如表:
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶液的体积(mL) | 20.05 | 20.00 | 18.80 | 19.95 |
(3)丙同学利用:5Fe2++MnO4-+8H+═5Fe3++Mn2++4H2O反应,用KMnO4溶液滴定某样品进行铁元素含量的测定.
①设计的下列滴定方式,最合理的是b.(夹持部分略去)(填字母序号)
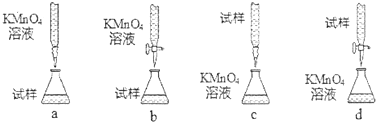
②判断滴定终点的依据是当滴下最后一滴KMnO4标准溶液时,溶液颜色变为浅紫红色,且在半分钟内不褪色.
分析 (1)硫酸亚铁易被氧化而变质,硫酸亚铁为强酸弱碱盐易水解,依据水解平衡影响因素解答;
(2)根据NaOH的体积,第3次数据显然误差较大,舍去;另外三次所用NaOH平均体积为20 mL,代入计算;
(3)①高锰酸钾具有强氧化性,能腐蚀碱式滴定管的橡皮管,应用酸式滴定管盛装,滴定时为便于观察颜色变化,滴定终点颜色由浅变深易于观察;
②根据KMnO4标准溶液本身就是一种指示剂.
解答 解:(1)硫酸亚铁易被氧化而生成硫酸铁,加入少量铁粉与三价铁离子反应生成二价铁离子,所以可以防止二价铁离子氧化;硫酸亚铁为强酸弱碱盐易水解生成硫酸和氢氧化亚铁,依据浓度对水解平衡影响,加入稀硫酸可以抑制二价铁子的水解;
故答案为:Fe;H2SO4;
(2)根据NaOH的体积,第3次数据显然误差较大,舍去;另外三次所用NaOH平均体积为20.00mL,
则醋酸溶液浓度=$\frac{0.2000mol/L×0.02L}{0.02L}$=0.2000 mol/L,
故答案为:0.2000 mol/L;
(3)①高锰酸钾具有强氧化性,能腐蚀碱式滴定管的橡皮管,应用酸式滴定管盛装,滴定时为便于观察颜色变化,滴定终点颜色由浅变深易于观察,应将高锰酸钾滴到待测液中,
故答案为:b;
②FeSO4反应完毕,加入最后一滴KMnO4溶液,溶液变为浅紫红色,浅紫红色半分钟内不褪去,说明滴定到终点;
故答案为:当滴下最后一滴KMnO4标准溶液时,溶液颜色变为浅紫红色,且在半分钟内不褪色.
点评 本题为综合题考查了盐类水解的应用,中和滴定、氧化还原反应滴定,明确盐类水解的规律,熟悉中和滴定、氧化还原滴定原理是解题关键,注意滴定数据的处理,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案
相关题目
12.已知某温度下,四种一元弱酸的电离平衡常数为:物质的量浓度都为0.1mol•L-1的下列溶液中,pH最小的是( )
| HCN | HF | CH3COOH | HNO2 | |
| Ka | 6.2×10-10 | 6.8×10-4 | 1.8×10-5 | 6.4×10-6 |
| A. | HCN | B. | CHSCOOH | C. | HF | D. | HNOp |
18.糖是体内的主要能源,人体所需的各种热量,70%由糖类提供.理论上,每摩尔葡萄糖在体内完全氧化时,释放的热量为2872kJ.葡萄糖完全氧化分解时的能量变化方程式为:
C6H12O6+6O2+38H3PO4+38ADP→6CO2+44H2O+38ATP
ATP+H2O→ADP+H3PO4,△H=-30.6kJ/mol
由此可知,人体内葡萄糖完全氧化分解时,能量的利用率为( )
C6H12O6+6O2+38H3PO4+38ADP→6CO2+44H2O+38ATP
ATP+H2O→ADP+H3PO4,△H=-30.6kJ/mol
由此可知,人体内葡萄糖完全氧化分解时,能量的利用率为( )
| A. | 40.5% | B. | 60.6% | C. | 81.0% | D. | 100% |
15.某温度下,在 2L 的密闭容器中,加入 1mol X(g)和 2mol Y(g)发生反应:X(g)+mY(g)?3Z(g)平衡时,X、Y、Z 的体积分数分别为 30%、60%、10%.在此平衡体系中加入 1mol Z(g),再次达到平衡后,X、Y、Z 的体积分数不变.下列叙述不正确的是( )
| A. | m=2 | |
| B. | X 与 Y 的平衡转化率之比为 1:2 | |
| C. | 两次平衡的平衡常数相同 | |
| D. | 第二次平衡时,Z 的浓度为 0.2 mol•L-1 |
17.在容积固定的密闭容器中存在如下反应:2A(g)+3B(g)?3C(g)△H<0某研究小组研究了当其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:
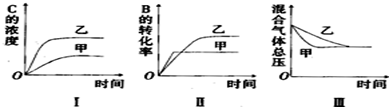
下列判断正确的是( )

下列判断正确的是( )
| A. | 图I研究的可能是不同催化剂对反应的影响,且乙使用的催化剂效率较高 | |
| B. | 图Ⅱ研究的可能是压强对反应的影响,且甲的压强较高 | |
| C. | 图Ⅱ研究的可能是温度对反应的影响,且甲的温度较高 | |
| D. | 图Ⅲ研究的可能是不同催化剂对反应的影响,且乙使用的催化剂效率较高 |
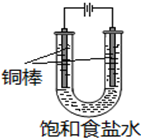 CuCl是应用广泛的有机合成催化剂,可采取不同方法制取.
CuCl是应用广泛的有机合成催化剂,可采取不同方法制取.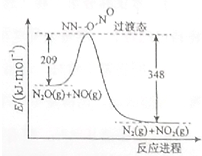 (1)硝酸铵加热分解可得到N2O和H2O,250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为NH4NO3$\stackrel{△}{?}$N2O+2H2O,平衡常数表达式为K=c(N2O)×c2(H2O);若有1mol硝酸铵完全分解,转移的电子数为4mol.
(1)硝酸铵加热分解可得到N2O和H2O,250℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为NH4NO3$\stackrel{△}{?}$N2O+2H2O,平衡常数表达式为K=c(N2O)×c2(H2O);若有1mol硝酸铵完全分解,转移的电子数为4mol.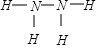 ,已知液态肼的标准燃烧热为-622kJ/mol,写出发生燃烧发生的热化学方程式:N2H4(l)+O2(g)=N2(g)+2H2O(l);△H=-622KJ/mol.
,已知液态肼的标准燃烧热为-622kJ/mol,写出发生燃烧发生的热化学方程式:N2H4(l)+O2(g)=N2(g)+2H2O(l);△H=-622KJ/mol.