题目内容
有A、B、C三种元素。已知:
①4 g A元素的单质与水作用,标准状况下放出H2 2.24 L,反应中有1.204×1023个电子发生转移;
②B元素可与A形成AB2型的离子化合物,且知A、B的离子具有相同的核外电子排布;
③元素C的气态氢化物可与其最高价氧化物的水化物发生非氧化还原反应生成盐,1 mol该盐含42个电子。
据此填写下列空白:
(1)元素符号:A__________,B__________,C__________。
(2)A元素的离子结构示意图:_____________。
(3)用电子式表示AB2的形成过程:__________________________________________。
(4)C的气态氢化物在催化剂作用下与O2反应的化学方程式:__________________________。
(5)用电子式表示C的气态氢化物的形成过程:_____________________________________。它与B的气态氢化物反应时有_________现象发生,生成物的电子式为:__________,它属于______晶体。
(1)Ca Cl N
(2)![]()
(3)![]()
(4)4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
(5)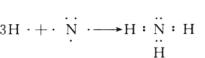 白烟
白烟
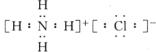 离子
离子
解析:由题知A元素为Ca、B元素为Cl、C元素为N,AB2型化合物为CaCl2,其为离子化合物。注意NH4Cl电子式的书写。

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目

