题目内容
4.由沸点数据:甲烷-146℃,乙烷-89℃,丁烷-0.5℃,戊烷36℃,可以判断丙烷的沸点可能是( )| A. | 高于-0.5℃ | B. | 约是+30℃ | C. | 约是-40℃ | D. | 低于-89℃ |
分析 由沸点数据:甲烷-146℃,乙烷-89℃,丁烷-0.5℃,戊烷36℃,根据这些数据知,烷烃中碳原子个数越多其熔沸点越高,据此分析解答.
解答 解:由沸点数据:甲烷-146℃,乙烷-89℃,丁烷-0.5℃,戊烷36℃,根据这些数据知,烷烃中碳原子个数越多其熔沸点越高,丙烷中含有3个碳原子,其原子个数大于乙烷而小于丁烷,所以其沸点应该大于乙烷而小于丙烷,则丙烷的沸点可能是约是-40℃,故选C.
点评 本题考查烷烃熔沸点比较,为高频考点,侧重考查学生分析判断及总结归纳能力,烷烃都是分子晶体,其熔沸点与相对分子质量成正比,题目难度不大.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
14.短周期元素W、X、Y和Z的原子序数依次增大.元素W是制备一种高效电池的重要材料,X原子的最外层电子数是内层电子数的2倍,元素Y是地壳中含量最丰富的金属元素,Z原子的最外层电子数是其电子层数的2倍.下列说法错误的是( )
| A. | 元素W、X的氯化物中,各原子均满足8电子的稳定结构 | |
| B. | 元素X的单质能与其最高价氧化物反应 | |
| C. | 元素Y的单质与氢氧化钠溶液或盐酸反应均有氢气生成 | |
| D. | 元素Z可与元素X形成共价化合物XZ2 |
15.氢有三种同位素:${\;}_{1}^{1}$H、${\;}_{1}^{2}$H和${\;}_{1}^{3}$H,它们之间存在差异的是( )
| A. | 中子数 | B. | 电子数 | C. | 原子序数 | D. | 质子数 |
19.在CuO和Fe粉的混合物中,加入一定量的稀硫酸,并微热,当反应停止后,滤出不溶物,向滤液中插入一枚铁钉,发现铁钉无任何变化.根据上述现象,确定下面结论正确的是( )
| A. | 不溶物只有铜 | |
| B. | 不溶物一定含铜,可能含铁 | |
| C. | 不溶物只有铁 | |
| D. | 溶液中一定含有Fe2+,可能含有Cu2+ |
13.下列各组晶体中化学键类型和晶体类型均相同的是( )
| A. | 二氧化硅和二氧化碳 | B. | 金刚石和石墨 | ||
| C. | 氯化钠和过氧化钠 | D. | 铁和铜 |
14.X、Y、Z三种短周期元素在周期表中的位置如图,X通过共用三对电子形成X2分子,下列说法不正确的是( )
| X | ||
| Y | Z |
| A. | 化合物XZ3中各原子均满足8电子的稳定结构 | |
| B. | X、Y、Z三种元素形成的含氧酸都是强酸 | |
| C. | 常温下,Z单质可与Y的氢化物发生置换反应 | |
| D. | Z的气态氢化物比Y的气态氢化物更加稳定 |
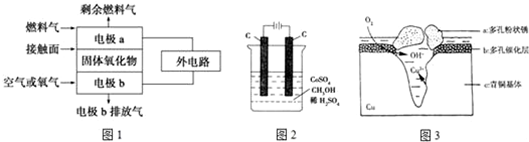
 ③能与水在一定条件下反应生成C
③能与水在一定条件下反应生成C