题目内容
11.下列性质递变规律正确的是( )| A. | 离子半径:K+>Cl->Na+>F- | B. | 酸性:H2SO4>H3PO4>H2CO3>H2SiO3 | ||
| C. | 熔点:石英>食盐>钾>干冰 | D. | 还原性:NaCl>NaBr>NaI>Na2S |
分析 A.电子层数越多,半径越大,具有相同电子数的离子,质子数越大,半径越小;
B.非金属性越强,最高价氧化物对应水化物的酸性越强;
C.熔点:原子晶体>离子晶体>分子晶体,K是金属晶体,熔点较低;
D.非金属性越强,阴离子的还原性越弱.
解答 解:A.K+与Cl-有3个电子层,Na+与F-有2个电子层,电子层数越多,半径越大,具有相同电子数的离子,质子数越大,半径越小,因此离子半径:Cl->K+>F->Na+,故A错误;
B.因非金属性:S>P>C>Si,故酸性:H2SO4>H3PO4>H2CO3>H2SiO3,故B正确;
C.石英是原子晶体,食盐是离子晶体、K是金属晶体、干冰是分子晶体,K是金属晶体,熔点较低,熔点:石英>食盐>钾>干冰,故C正确;
D.因非金属性Cl>Br>I>S,故还原性:Na2S>NaI>NaBr>NaCl,故D错误;
故选BC.
点评 本题考查了微粒半径大小比较、金属性和非金属性、晶体熔点高低等方面知识,综合性强,明确常见的比较的方法是解答本题的关键,注意知识的归纳整理,题目难度不大.

练习册系列答案
相关题目
1.类比归纳是学习化学的重要方法,对如下类比的说法正确的是( )
| A. | NO2、SO2都是酸性氧化物,都能使酸性高锰酸钾溶液褪色 | |
| B. | MgO、Al2O3都是高熔点离子化合物,都能用作耐热材料 | |
| C. | CO2与SiO2化学式相似,则CO2与SiO2的物理性质也相似 | |
| D. | CuO、Fe2O3都是不溶于水的碱性氧化物,都是黑色粉末 |
2.《中华人民共和国大气污染防治法》于2016年1月1日起实施.为保护和改善大气环境,下列做法不应该提倡的是( )
| A. | 开发生物质能替代化石燃料 | B. | 向高空排放金属冶炼产生的粉尘 | ||
| C. | 用催化转化技术处理汽车尾气 | D. | 大力推广生产和使用无氟冰箱 |
6.短周期元素甲、乙、丙、丁的原子序数依次增大,甲位于第VA族,乙原子的核外电子数比甲原子多1,乙与丁同族,丙原子最外层电子数与电子层数相等.下列判断正确的是( )
| A. | 离子半径:丁>丙>乙 | |
| B. | 81号元素铊与丙元素处同主族,则铊的最高价氧化物对应水化物呈两性 | |
| C. | 电解法可以用乙与丙形成的化合物制得丙单质 | |
| D. | 同周期元素中丁的最高价氧化物对应水化物的酸性最强 |
16. 氮可形成多种气态氧化物,如NO、NO2、N2O4等.已知NO2和N2O4的结构式分别是
氮可形成多种气态氧化物,如NO、NO2、N2O4等.已知NO2和N2O4的结构式分别是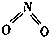 和
和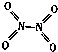 .实验测得N-N键的键能为167kJ•mol-1,NO2中氮氧键的键能为 466kJ•mol-1,N2O4中氮氧键的键能为438.5kJ•mol-1.
.实验测得N-N键的键能为167kJ•mol-1,NO2中氮氧键的键能为 466kJ•mol-1,N2O4中氮氧键的键能为438.5kJ•mol-1.
(1)写出N2O4转化NO2为的热化学方程式N2O4(g)?2NO2(g)△H=+57 kJ•mol-1.
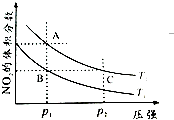
(2)对反应N2O4(g)?2NO2(g),在温度T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.
①A、C两点的反应速率v(A)<v(C)(填“>”“=”或“<”).
②B、C两点的气体平均相对分子质量M(B)=M(C)(填“>”、“=”或“<”).
③由状态B到达状态A可用的方法是加热.
④A点气体的颜色比C点浅(填“深”、“浅”或“相同”),原因是A点到C点时压强增大,即体积减小,平衡逆移,NO2的体积分数减小,但平衡时C点c(NO2)比A点大.
(3)在100℃时,将0.40mol的NO2气体充入2L的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到下表所示数据.
①在上述条件下,从反应开始直至20s时,v(NO2)=0.0025mol•L-1•s-1.
②若在相同的情况下最初向该容器充入的是N2O4气体,要达到上述同样的平衡状态,N2O4的起始浓度应是0.10 mol•L-1.
 氮可形成多种气态氧化物,如NO、NO2、N2O4等.已知NO2和N2O4的结构式分别是
氮可形成多种气态氧化物,如NO、NO2、N2O4等.已知NO2和N2O4的结构式分别是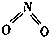 和
和 .实验测得N-N键的键能为167kJ•mol-1,NO2中氮氧键的键能为 466kJ•mol-1,N2O4中氮氧键的键能为438.5kJ•mol-1.
.实验测得N-N键的键能为167kJ•mol-1,NO2中氮氧键的键能为 466kJ•mol-1,N2O4中氮氧键的键能为438.5kJ•mol-1.(1)写出N2O4转化NO2为的热化学方程式N2O4(g)?2NO2(g)△H=+57 kJ•mol-1.
(2)对反应N2O4(g)?2NO2(g),在温度T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.
①A、C两点的反应速率v(A)<v(C)(填“>”“=”或“<”).
②B、C两点的气体平均相对分子质量M(B)=M(C)(填“>”、“=”或“<”).
③由状态B到达状态A可用的方法是加热.
④A点气体的颜色比C点浅(填“深”、“浅”或“相同”),原因是A点到C点时压强增大,即体积减小,平衡逆移,NO2的体积分数减小,但平衡时C点c(NO2)比A点大.
(3)在100℃时,将0.40mol的NO2气体充入2L的密闭容器中,每隔一定时间就对该容器内的物质进行分析,得到下表所示数据.
| 时间/s | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
②若在相同的情况下最初向该容器充入的是N2O4气体,要达到上述同样的平衡状态,N2O4的起始浓度应是0.10 mol•L-1.
20.下列物质中,常温下既能跟盐酸反应,又能跟NaOH溶液反应的是( )
| A. | MgO | B. | Al2O3 | C. | SiO2 | D. | Cl2 |
1.关于硅及其化合物的用途,不正确的是( )
| A. | 硅胶可用作干燥剂 | |
| B. | 二氧化硅可用作计算机的芯片 | |
| C. | 硅酸钠是制备木材防火剂的原料 | |
| D. | 用纯碱、石灰石、石英为原料可制普通玻璃 |