题目内容
一定条件下,在容积固定的某密闭容器中发生的反应N2+3H2?2NH3.在10s内N2的浓度由5mol/L降至4mol/L.下列说法正确的是 ( )
| A、用NH3表示的化学反应速率为0.1 mol/(L?s) |
| B、维持容积的体积不变充入氩气,会加快该反应的速率 |
| C、增加H2的浓度该正反应速率和逆反应速率都会加快 |
| D、反应足够长时间,N2、H2中至少有一种物质浓度降为零 |
考点:化学平衡建立的过程
专题:化学平衡专题
分析:A、根据v=
计算出氮气的速率,再根据速率之比等于计量数之比求得氨气的反应速率;
B、容积不变加入氩气,反应中的各物质的浓度不变,所以化学反应速率不变;
C、增加H2的浓度正反应速率加快,随着生成物浓度的增加逆反应速率也会加快;
D、该反应为可逆反应,根据可逆反应的特点,反应物的浓度不可能降为零的;
| △c |
| t |
B、容积不变加入氩气,反应中的各物质的浓度不变,所以化学反应速率不变;
C、增加H2的浓度正反应速率加快,随着生成物浓度的增加逆反应速率也会加快;
D、该反应为可逆反应,根据可逆反应的特点,反应物的浓度不可能降为零的;
解答:
解:A、根据v=
计算出氮气的速率为
=0.1 mol/(L?s),再根据速率之比等于计量数之比求得氨气的反应速率为2×0.1 mol/(L?s)=0.2mol/(L?s),故A错误;
B、容积不变加入氩气,反应中的各物质的浓度不变,所以化学反应速率不变,故B错误;
C、增加H2的浓度该正反应速率加快,随着生成物浓度的增加逆反应速率也会加快,故C正确;
D、该反应为可逆反应,根据可逆反应的特点,反应物的浓度不可能降为零的,故D错误;
故选C.
| △c |
| t |
| 5mol/L-4mol/L |
| 10s |
B、容积不变加入氩气,反应中的各物质的浓度不变,所以化学反应速率不变,故B错误;
C、增加H2的浓度该正反应速率加快,随着生成物浓度的增加逆反应速率也会加快,故C正确;
D、该反应为可逆反应,根据可逆反应的特点,反应物的浓度不可能降为零的,故D错误;
故选C.
点评:本题主要考查了反应速率的计算、影响平衡移动的因素、及可逆反应的特征等知识点,难度不大,解题时注意基础知识的灵活运用.

练习册系列答案
 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
硫酸是一种重要的化工产品,目前主要采用“接触法”进行生产.有关接触氧化反应2SO2+O2
2SO3的说法中正确的是( )
| 催化剂 |
| △ |
| A、只要选择适宜的条件,SO2和O2就能全部转化为SO3 |
| B、该反应达到平衡后,反应就完全停止了,即正逆反应速率为零 |
| C、若用18O原子组成的O2参加反应,平衡时SO2中也会含有18O |
| D、在工业合成SO3时,要同时考虑反应速率和反应能达到的限度两方面的问题 |
下列各组物质互为同系物的是( )
| A、苯酚和苯甲醇 |
| B、甲醇和乙二醇 |
| C、甲酸和硬脂酸 |
| D、一氯甲烷和二氯甲烷 |
乙烯和乙醇的混合气体V L,完全燃烧消耗相同状态下的氧气3V L,则混合气体中乙烯和乙醇的体积比为( )
| A、1:1 | B、2:1 |
| C、1:2 | D、任意比 |
海水中蕴藏着丰富的资源.海水综合利用的示意图如图.下列说法正确的是( )


| A、通过氯碱工业可生产的产品有NaOH、NaClO、盐酸等 |
| B、卤水经过蒸发结晶可直接得到较纯净的MgCl2?6H2O晶体 |
| C、粗盐精制的过程只发生物理变化 |
| D、在高温下用氢气还原MgCl2可制取金属镁 |
下列溶液通入过量的CO2后无沉淀有的( )
| A、CaCl2 |
| B、Ca(ClO)2 |
| C、Na2SiO3 |
| D、饱和Na2CO3溶液 |
下列说法正确的是( )
| A、碘晶体受热转变成碘蒸气,吸收的热量用于克服碘原子间的作用力 |
| B、分子晶体中都存在共价键 |
| C、氯化氢和氯化钾的溶解克服相同类型作用力 |
| D、在晶体中只要有阴离子就一定有阳离子 |
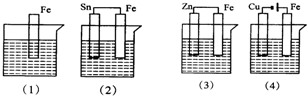 如图各容器中盛有海水,铁在其中腐蚀时由快到慢的顺序是( )
如图各容器中盛有海水,铁在其中腐蚀时由快到慢的顺序是( )| A、(4)>(2)>(1)>(3) |
| B、(2)>(1)>(3)>(4) |
| C、(4)>(2)>(3)>(1) |
| D、(3)>(2)>(4)>(1) |