题目内容
写出下列反应的离子或化学方程式
①写出氢氧化铜与稀硫酸反应的离子方程式: .
②写出碳酸氢钠与稀盐酸反应的离子方程式: .
③写出离子方程式H++OH-=H2O相对应的一个化学方程式: .
④写出铁与硫酸铜溶液反应的离子方程式: .
⑤写出离子方程式Ag++Cl-=AgCl↓相对应的一个化学方程式: .
①写出氢氧化铜与稀硫酸反应的离子方程式:
②写出碳酸氢钠与稀盐酸反应的离子方程式:
③写出离子方程式H++OH-=H2O相对应的一个化学方程式:
④写出铁与硫酸铜溶液反应的离子方程式:
⑤写出离子方程式Ag++Cl-=AgCl↓相对应的一个化学方程式:
考点:离子方程式的书写,化学方程式的书写
专题:
分析:①氢氧化铜与稀硫酸反应生成硫酸铜和水;
②碳酸氢钠与稀盐酸反应生成二氧化碳、水和氯化钠;
③离子方程式H++OH-=H2O表示强酸与强碱反应生成可溶性盐;
④铁与硫酸铜溶液反应生成铜和酸亚铁;
⑤离子方程式Ag++Cl-=AgCl↓,表示硝酸银与可溶性盐酸盐或者盐酸反应.
②碳酸氢钠与稀盐酸反应生成二氧化碳、水和氯化钠;
③离子方程式H++OH-=H2O表示强酸与强碱反应生成可溶性盐;
④铁与硫酸铜溶液反应生成铜和酸亚铁;
⑤离子方程式Ag++Cl-=AgCl↓,表示硝酸银与可溶性盐酸盐或者盐酸反应.
解答:
解:①氢氧化铜与稀硫酸反应的离子方程式:Cu(OH)2+2H+═Cu2++2H2O;
故答案为:Cu(OH)2+2H+═Cu2++2H2O;
②碳酸氢钠与稀盐酸反应的离子方程式:H++HCO3-=H2O+CO2↑;
故答案为:H++HCO3-=H2O+CO2↑;
③离子方程式H++OH-=H2O可以表示盐酸与氢氧化钠反应,化学方程式为:HCl+NaOH=NaCl+H2O,
故答案为:HCl+NaOH=NaCl+H2O;
④铁与硫酸铜溶液反应的离子方程式:Fe+Cu2+=Cu+Fe2+;
故答案为:Fe+Cu2+=Cu+Fe2+;
⑤离子方程式Ag++Cl-=AgCl↓可以表示硝酸银与盐酸反应,化学方程式为:AgNO3+HCl=AgCl↓+HNO3;
故答案为:AgNO3+HCl=AgCl↓+HNO3.
故答案为:Cu(OH)2+2H+═Cu2++2H2O;
②碳酸氢钠与稀盐酸反应的离子方程式:H++HCO3-=H2O+CO2↑;
故答案为:H++HCO3-=H2O+CO2↑;
③离子方程式H++OH-=H2O可以表示盐酸与氢氧化钠反应,化学方程式为:HCl+NaOH=NaCl+H2O,
故答案为:HCl+NaOH=NaCl+H2O;
④铁与硫酸铜溶液反应的离子方程式:Fe+Cu2+=Cu+Fe2+;
故答案为:Fe+Cu2+=Cu+Fe2+;
⑤离子方程式Ag++Cl-=AgCl↓可以表示硝酸银与盐酸反应,化学方程式为:AgNO3+HCl=AgCl↓+HNO3;
故答案为:AgNO3+HCl=AgCl↓+HNO3.
点评:本题考查了离子方程式的书写,题目难度不大,明确反应的实质是将解题关键,注意电荷守恒、原子个数守恒.

练习册系列答案
相关题目
下列反应属于置换反应的是( )
| A、NH4Cl=NH3↑+HCl↑ |
| B、NaCl+AgNO3=AgCl↓+NaNO3 |
| C、CaO+CO2=CaCO3 |
| D、Mg+2HCl=MgCl2+H2↑ |
下列氧化还原反应发生在同种元素之间的是( )
| A、Zn+2 HCl═ZnCl2+H2↑ | ||||
| B、2 H2S+SO2═3S↓+2 H2O | ||||
C、H2+CuO
| ||||
D、2 H2O
|
NA表示阿伏加德罗常数,以下说法正确的是( )
| A、在通常条件下,1mol氩气含有的原子数为2NA |
| B、56g金属铁由原子变为离子时失去的电子数为NA |
| C、在标准状况下,2.24 L氨气所含的电子总数约为NA |
| D、1 mol/L 的 Na2SO4溶液中含有Na+个数为2NA |
下列离子方程式正确的是( )
| A、铁和硝酸银溶液反应 Fe+Ag+=3Ag+Fe3+ |
| B、氢氧化镁与硫酸溶液反应 OH-+H+=H2O |
| C、铁与稀硫酸反应 2Fe+6H+=2Fe3++3H2↑ |
| D、碳酸钙与盐酸反应 CaCO3+2H+=Ca2++CO2↑+H2O |
关于KOH溶液和Fe(OH)3胶体描述正确的是( )
| A、两者的分散质都属于碱 |
| B、两者均为有色不透明的分散系 |
| C、两者分散质的直径都介于10-9~10-7m之间 |
| D、两者都有丁达尔效应 |
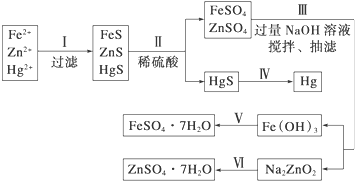 某工厂排出的污水中含有大量的Fe3+、Zn2+、Hg2+三种金属离子.以下是某化学研究性学习小组的同学设计除去污水中的金属离子,并回收绿矾、皓矾(ZnSO4?7H2O)和汞的方案.
某工厂排出的污水中含有大量的Fe3+、Zn2+、Hg2+三种金属离子.以下是某化学研究性学习小组的同学设计除去污水中的金属离子,并回收绿矾、皓矾(ZnSO4?7H2O)和汞的方案.