��Ŀ����
���Ż�����ʶ����ǿ�������ԴԽ��Խ�����ǹ�ע��
��1�������ڶ�ʮһ�����п�����������Դ��̨�ϳ�Ϊһ�־������صĶ�����Դ��
����-��ѭ���ֽ�ˮ������Ҫ�漰���з�Ӧ��
I��SO2+2H2O+I2�TH2SO4+2HI
��2HI?H2+I2
��2H2SO4�T2SO2+O2+2H2O
����������Ӧ�������ж���ȷ���� ������ţ���ͬ����
a����Ӧ����һ�����ȷ�Ӧ b���ڸ�ѭ�������У��и�������������
c���ɷ�Ӧ����жϣ�HI��̫�ȶ� d��ѭ�������в���1 mol O2��ͬʱ����44.8L H2
�����ü�����ˮ��Ӧ�Ʊ���������ԭ�ϼ��������ʸߣ�����ʵ���ƹ��ֵ����֪�÷�ӦΪ��
��CH4��g��+H2O��g��?CO��g��+3H2��g����H=+206.2kJ/mol
��CH4��g��+2H2O��g��?CO2��g��+4H2��g����H=+165.0kJ/mol
������Ӧ����ԭ�����е�CO��ʹ���ϳɴ����ж��������ȥ����ҵ�ϳ����ô���������CO��ˮ������Ӧ�����׳�ȥ��CO2��ͬʱ�ֿ��Ƶõ�����������ķ������˷�Ӧ��Ϊһ����̼�任��Ӧ���÷�Ӧ���Ȼ�ѧ����ʽ�� ��
��800��ʱ����Ӧ���ƽ�ⳣ��K1=1.0��ijʱ�̲�ø��¶��£��ܱ������и����ʵ����ʵ���Ũ�ȷֱ�Ϊ��c��CH4��=2.0mol?L-1��c��H2O��=5.0mol?L-1��c��CO��=2.0mol?L-1��c��H2��=2.5mol?L-1�����ʱ���淴Ӧ���ʵĹ�ϵ��v�� �����������������=����v����
��2���״���һ�ֿ�������Դ�����п�����Ӧ�õĹ���ǰ������ҵ��һ��ɲ������·�Ӧ���ϳɼ״���CO��g��+2H2��g��?CH3OH��g���������÷�Ӧ���ش��������⣺
��һ�������£���CO��H2�������1��1�����ܱ������з������Ϸ�Ӧ����˵���÷�Ӧ�Ѵﵽƽ����� ��
a����ϵ��ѹǿ�������仯 b��CO��H2������ȱ��ֲ���
c����ϵ��̼Ԫ�صİٷֺ������ٱ仯 d����λʱ��������1mol CO��ͬʱ����1mol CH3OH
����ͼ1�Ǹ÷�Ӧ�ڲ�ͬ�¶���CO��ת������ʱ��仯�����ߣ�T1��T2�¶��µ�ƽ�ⳣ����С��ϵ��K1 �����������������=���� K2�������ǣ� ��
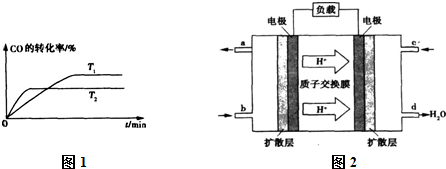
����֪�״�ȼ�ϵ�صĹ���ԭ����ͼ2��ʾ��
�õ�ع���ʱ���õ���ұߵĵ缫�����ĵ缫��Ӧ�� ������һ��ʱ�����3mol���ӷ���ת��ʱ�����ɱ�״���µ����� L��
��1�������ڶ�ʮһ�����п�����������Դ��̨�ϳ�Ϊһ�־������صĶ�����Դ��
����-��ѭ���ֽ�ˮ������Ҫ�漰���з�Ӧ��
I��SO2+2H2O+I2�TH2SO4+2HI
��2HI?H2+I2
��2H2SO4�T2SO2+O2+2H2O
����������Ӧ�������ж���ȷ����
a����Ӧ����һ�����ȷ�Ӧ b���ڸ�ѭ�������У��и�������������
c���ɷ�Ӧ����жϣ�HI��̫�ȶ� d��ѭ�������в���1 mol O2��ͬʱ����44.8L H2
�����ü�����ˮ��Ӧ�Ʊ���������ԭ�ϼ��������ʸߣ�����ʵ���ƹ��ֵ����֪�÷�ӦΪ��
��CH4��g��+H2O��g��?CO��g��+3H2��g����H=+206.2kJ/mol
��CH4��g��+2H2O��g��?CO2��g��+4H2��g����H=+165.0kJ/mol
������Ӧ����ԭ�����е�CO��ʹ���ϳɴ����ж��������ȥ����ҵ�ϳ����ô���������CO��ˮ������Ӧ�����׳�ȥ��CO2��ͬʱ�ֿ��Ƶõ�����������ķ������˷�Ӧ��Ϊһ����̼�任��Ӧ���÷�Ӧ���Ȼ�ѧ����ʽ��
��800��ʱ����Ӧ���ƽ�ⳣ��K1=1.0��ijʱ�̲�ø��¶��£��ܱ������и����ʵ����ʵ���Ũ�ȷֱ�Ϊ��c��CH4��=2.0mol?L-1��c��H2O��=5.0mol?L-1��c��CO��=2.0mol?L-1��c��H2��=2.5mol?L-1�����ʱ���淴Ӧ���ʵĹ�ϵ��v��
��2���״���һ�ֿ�������Դ�����п�����Ӧ�õĹ���ǰ������ҵ��һ��ɲ������·�Ӧ���ϳɼ״���CO��g��+2H2��g��?CH3OH��g���������÷�Ӧ���ش��������⣺
��һ�������£���CO��H2�������1��1�����ܱ������з������Ϸ�Ӧ����˵���÷�Ӧ�Ѵﵽƽ�����
a����ϵ��ѹǿ�������仯 b��CO��H2������ȱ��ֲ���
c����ϵ��̼Ԫ�صİٷֺ������ٱ仯 d����λʱ��������1mol CO��ͬʱ����1mol CH3OH
����ͼ1�Ǹ÷�Ӧ�ڲ�ͬ�¶���CO��ת������ʱ��仯�����ߣ�T1��T2�¶��µ�ƽ�ⳣ����С��ϵ��K1

����֪�״�ȼ�ϵ�صĹ���ԭ����ͼ2��ʾ��
�õ�ع���ʱ���õ���ұߵĵ缫�����ĵ缫��Ӧ��
���㣺ת�������¶ȡ�ѹǿ�ı仯����,������ѧ��Դ�����༰�乤��ԭ��,��ѧƽ�⽨���Ĺ���,��ѧƽ���Ӱ������
ר�⣺��ѧƽ��ר��,�绯ѧר��
��������1����a�����᳣���²��ֽ⣮
b�����ݷ�Ӧ��������Ƿ�Ӧ���������������жϣ�
c�����ݷ�Ӧ2HI?H2+I2֪��HI��̫�ȶ���
d���ɢ��֪����lmolO2��ͬʱ����2molSO2����I��֪2molSO2����4molHI���ɢ��֪4molHI�ֽ�����2mol H2��
�ڸ��ݸ�˹���������Ȼ�ѧ����ʽ�ĺ��������㷴Ӧ���ʱ䣻����Ũ���̺�ƽ�ⳣ���Ĺ�ϵ��ȷ���ƶ�����
��2���ٵ���Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�Ȳ��ٸı䣬�ɴ�������һЩ������Ҳ���䣬�Դ˽����жϣ�
���ɴﵽƽ������Ҫ��ʱ�䳤��֪�¶ȵĴ�С��ϵ�������¶ȶ�ƽ���ƶ���Ӱ�����ش��жϣ�
�۸���ȼ�ϵ�صĹ���ԭ���Լ������غ�˼�����ش���㣮
b�����ݷ�Ӧ��������Ƿ�Ӧ���������������жϣ�
c�����ݷ�Ӧ2HI?H2+I2֪��HI��̫�ȶ���
d���ɢ��֪����lmolO2��ͬʱ����2molSO2����I��֪2molSO2����4molHI���ɢ��֪4molHI�ֽ�����2mol H2��
�ڸ��ݸ�˹���������Ȼ�ѧ����ʽ�ĺ��������㷴Ӧ���ʱ䣻����Ũ���̺�ƽ�ⳣ���Ĺ�ϵ��ȷ���ƶ�����
��2���ٵ���Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�Ȳ��ٸı䣬�ɴ�������һЩ������Ҳ���䣬�Դ˽����жϣ�
���ɴﵽƽ������Ҫ��ʱ�䳤��֪�¶ȵĴ�С��ϵ�������¶ȶ�ƽ���ƶ���Ӱ�����ش��жϣ�
�۸���ȼ�ϵ�صĹ���ԭ���Լ������غ�˼�����ش���㣮
���
�⣺��1����a�����᳣�����ȶ������ֽ⣬��a��ȷ��
b����Ӧ��������Ƿ�Ӧ�����������ֻ�����Ƿ�Ӧ�е��м������ѣ���b����
c�����ݷ�Ӧ2HI?H2+I2����Ӧ�ǿ���ģ�֪��HI��̫�ȶ�����c��ȷ��
d���ɢ��֪����lmolO2��ͬʱ����2molSO2����I��֪2molSO2����4molHI���ɢ��֪4molHI�ֽ�����2molH2������ֻ���ڱ���µ��������44.8L����d����
��ѡac��
����֪����CH4��g��+H2O��g��?CO��g��+3H2��g����H=+206.2kJ/mol
��CH4��g��+2H2O��g��?CO2��g��+4H2��g����H=+165.0kJ/mol�����ݸ�˹���ɣ���ӦCO��g��+H2O��g��?CO2��g��+H2��g�������Ǣ�-��õ������ԡ�H=165.0kJ/mol-206.2kJ/mol=-41.2 kJ/mol��800��ʱ����Ӧ���ƽ�ⳣ��K1=1.0��ijʱ�̲�ø��¶��£��ܱ������и����ʵ����ʵ���Ũ�ȷֱ�Ϊ��c��CH4��=2.0mol?L-1��c��H2O��=5.0mol?L-1��c��CO��=2.0mol?L-1��c��H2��=2.5mol?L-1����Qc=
=
��1�����Ի�ѧ��Ӧ������в��ܴﵽƽ�⣬
��v����v�����ʴ�Ϊ��CO��g��+H2O��g��?CO2��g��+H2��g����H=-41.2 kJ/mol������
��2����a��CO��g��+2H2��g��?CH3OH��g����һ����Ӧǰ�����������С�ķ�Ӧ���ʵ�ѹǿ����ʱ������Ӧ�ﵽƽ�⣬��a��ȷ��
b��CO��H2������ȱ��ֲ���ʱ��˵��ƽ�ⲻ���ƶ�����b��ȷ��
c�����������غ㣬��ϵ��̼Ԫ�صİٷֺ�������仯����c����
d���κ�����£���λʱ��������1 mol CO��ͬʱ����l mol CH3OH����d����
��ѡab��
���ɴﵽƽ������Ҫ��ʱ�䳤��֪��T1��T2�����¶���T2��T1�����£�ʱ��CO��ת��������˵�������¶�ʱƽ�������ƶ���������Ӧ�Ƿ��ȷ�Ӧ����H��0��K1��K2���ʴ�Ϊ��������ͼ���¶���T1������T2ʱ��CO��ת���ʽ��ͣ�˵��ƽ�����淴Ӧ�����ƶ�������K1��K2��
�۸���H+�˶�����d���ų�H2O֪����b�ڽ���������Ǽ״�����c�ڽ����������O2�����ڵ������Һ���ᣬ��������ӦΪO2+4H++4e-=2H2O������3mol���ӷ���ת��ʱ����0.5mol�״���Ӧ�����ɶ�����̼Ϊ0.5mol�ڱ�״���µ����� 11.2L��
�ʴ�Ϊ��O2+4H++4e-=2H2O��11.2��
b����Ӧ��������Ƿ�Ӧ�����������ֻ�����Ƿ�Ӧ�е��м������ѣ���b����
c�����ݷ�Ӧ2HI?H2+I2����Ӧ�ǿ���ģ�֪��HI��̫�ȶ�����c��ȷ��
d���ɢ��֪����lmolO2��ͬʱ����2molSO2����I��֪2molSO2����4molHI���ɢ��֪4molHI�ֽ�����2molH2������ֻ���ڱ���µ��������44.8L����d����
��ѡac��
����֪����CH4��g��+H2O��g��?CO��g��+3H2��g����H=+206.2kJ/mol
��CH4��g��+2H2O��g��?CO2��g��+4H2��g����H=+165.0kJ/mol�����ݸ�˹���ɣ���ӦCO��g��+H2O��g��?CO2��g��+H2��g�������Ǣ�-��õ������ԡ�H=165.0kJ/mol-206.2kJ/mol=-41.2 kJ/mol��800��ʱ����Ӧ���ƽ�ⳣ��K1=1.0��ijʱ�̲�ø��¶��£��ܱ������и����ʵ����ʵ���Ũ�ȷֱ�Ϊ��c��CH4��=2.0mol?L-1��c��H2O��=5.0mol?L-1��c��CO��=2.0mol?L-1��c��H2��=2.5mol?L-1����Qc=
| c(CO)?c3(H2) |
| c(CH4)?c(H2O) |
| 2.0��2��53 |
| 2.0��5.0 |
��v����v�����ʴ�Ϊ��CO��g��+H2O��g��?CO2��g��+H2��g����H=-41.2 kJ/mol������
��2����a��CO��g��+2H2��g��?CH3OH��g����һ����Ӧǰ�����������С�ķ�Ӧ���ʵ�ѹǿ����ʱ������Ӧ�ﵽƽ�⣬��a��ȷ��
b��CO��H2������ȱ��ֲ���ʱ��˵��ƽ�ⲻ���ƶ�����b��ȷ��
c�����������غ㣬��ϵ��̼Ԫ�صİٷֺ�������仯����c����
d���κ�����£���λʱ��������1 mol CO��ͬʱ����l mol CH3OH����d����
��ѡab��
���ɴﵽƽ������Ҫ��ʱ�䳤��֪��T1��T2�����¶���T2��T1�����£�ʱ��CO��ת��������˵�������¶�ʱƽ�������ƶ���������Ӧ�Ƿ��ȷ�Ӧ����H��0��K1��K2���ʴ�Ϊ��������ͼ���¶���T1������T2ʱ��CO��ת���ʽ��ͣ�˵��ƽ�����淴Ӧ�����ƶ�������K1��K2��
�۸���H+�˶�����d���ų�H2O֪����b�ڽ���������Ǽ״�����c�ڽ����������O2�����ڵ������Һ���ᣬ��������ӦΪO2+4H++4e-=2H2O������3mol���ӷ���ת��ʱ����0.5mol�״���Ӧ�����ɶ�����̼Ϊ0.5mol�ڱ�״���µ����� 11.2L��
�ʴ�Ϊ��O2+4H++4e-=2H2O��11.2��
����������Ŀ�ۺϿ���ѧ���й��Ȼ�ѧ���绯ѧ�Լ���ѧ��Ӧ���ʺͻ�ѧƽ���ƶ����й�֪ʶ�������ۺ�֪ʶ�Ŀ��飬�Ѷȴ�

��ϰ��ϵ�д�
�����Ŀ
����������ˮ��Ӧ������������ԭ��Ӧ���ǣ�������
| A��NO2 |
| B��CaO |
| C��Cl2 |
| D��Na2O2 |
��һ���¶��¿��淴ӦH2��g��+I2��g��?2HI��g���ﵽƽ��ı�־�ǣ�������
| A����λʱ���ڷ�Ӧ��nmolI2ͬʱ����2nmolHI |
| B����1molH-H�����ѣ�ͬʱ��1molI-I���γ� |
| C��������ѹǿ������ʱ����仯 |
| D��H2��I2��HI��Ũ��֮��Ϊ1��1��2 |

