题目内容
从海水中提取溴有如下反应:5NaBr+NaBrO3+3H2SO4=3Br2+3Na2SO4+3H2O,与上述反应在氧化还原原理上最相似的反应是( )
| A、2NaBr+Cl2═2NaCl+Br2 | ||||
B、2KMnO4
| ||||
| C、2H2S+SO2═3S↓+2H2O | ||||
| D、2FeCl3+H2S═2FeCl2+S↓+2HCl |
考点:氧化还原反应
专题:氧化还原反应专题
分析:NaBr中的溴元素化合价为-1价,NaBrO3中溴元素的化合价为+5价,最后都生成了0价的溴单质,属于氧化还原反应中的归中反应类型.
解答:
解:A.化合价变化的分别是溴元素和氯元素,不是归中反应类型,故A错误;
B.该反应中化合价变化的是Mn、O元素,所以不是归中反应类型,故B错误;
C.硫元素的化合价从-2价升到0价,还有的从+4价降到0价,属于氧化还原反应中的归中反应类型,故C正确;
D.该反应中化合价变化的是Fe、S元素,所以不是归中反应类型,故D错误;
故选C.
B.该反应中化合价变化的是Mn、O元素,所以不是归中反应类型,故B错误;
C.硫元素的化合价从-2价升到0价,还有的从+4价降到0价,属于氧化还原反应中的归中反应类型,故C正确;
D.该反应中化合价变化的是Fe、S元素,所以不是归中反应类型,故D错误;
故选C.
点评:本题考查了氧化还原反应,根据元素化合价变化及反应类型确定即可,知道常见元素化合价是解本题关键,题目难度不大.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
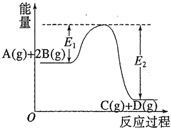 反应A(g)+2B(g)?C(g)+D(g)过程中的能量变化如图所示,有关叙述正确的是( )
反应A(g)+2B(g)?C(g)+D(g)过程中的能量变化如图所示,有关叙述正确的是( )| A、该反应是吸热反应 |
| B、当反应达到平衡时,升高温度,A的转化率增大 |
| C、反应体系中加入催化剂对反应热无影响 |
| D、在反应体系中加入催化剂,反应速率增大,E1减小,E2不变 |
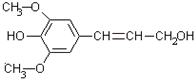 膳食纤维具有突出保健功能,近年来受到人们的普遍关注,被世界卫生组织称为人体的“第七营养素”.木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构如图,下列有关芥子醇说法正确的是( )
膳食纤维具有突出保健功能,近年来受到人们的普遍关注,被世界卫生组织称为人体的“第七营养素”.木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构如图,下列有关芥子醇说法正确的是( )| A、芥子醇的分子式是C11H12O4 |
| B、芥子醇能与FeCl3溶液发生显色反应 |
| C、芥子醇分子中所有碳原子不可能在同一平面 |
| D、1mol芥子醇能与足量溴水反应消耗1molBr2 |
某气态烃0.5mol能与1mol氯化氢完全加成,加成后的产物分子上的氢原子最多可被3mol氯气取代,则此气态烃可能是( )
| A、CH2=CH2 |
| B、CH2=C(CH3)-CH3 |
| C、CH≡CH |
| D、CH≡C-CH3 |
含氢氧化钠0.25mol的稀溶液与足量的稀盐酸反应,放出14.35kJ的热量,表示该反应的热化学方程式是( )
| A、NaOH (aq)+HCl (aq)═NaCl (aq)+H2O (l)△H=-14.35 kJ?mol-1 |
| B、NaOH (aq)+HCl (aq)═NaCl (aq)+H2O (l)△H=-28.70 kJ?mol-1 |
| C、NaOH+HCl═NaCl+H2O△H=-57.40 kJ?mol-1 |
| D、NaOH (aq)+HCl (aq)═NaCl (aq)+H2O (l)△H=-57.40 kJ?mol-1 |
一定条件下,在体积为10L的密闭容器中,1mol X和1mol Y进行反应:2X(g)+Y(g)?Z(g),经60s达到平衡,生成0.3mol Z,下列说法正确的是( )
| A、达到平衡时X浓度为0.04 mol/L |
| B、将容器体积变为20L,Z的平衡浓度变为0.015mol/L |
| C、若增大压强,平衡向正反应方向移动,平衡常数变大 |
| D、若升高温度,X的体积分数增大,则该反应的△H<0 |
下列说法中正确的是( )
| A、某无色溶液中可能含有下列离子:H+、Cl-、Na+、Fe2+ |
| B、能使石蕊变红的溶液中可能含有Cl-、K+、Na+、NO3- |
| C、取少量某溶液,向其中加入盐酸酸化的BaCl2溶液,通过观察是否有白色沉淀生成,可证明该溶液中是否含有SO42- |
| D、H++OH-═H2O可描述所有酸碱中和反应的实质 |
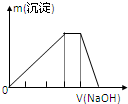 某盐A是含有两种阳离子的硫酸盐,将该溶液溶于水,向溶液中滴加NaOH溶液生成沉淀的物质的量与NaOH体积关系如图所示,下列离子溶液中能大量共存,加入晶体A后仍能大量共存的是( )
某盐A是含有两种阳离子的硫酸盐,将该溶液溶于水,向溶液中滴加NaOH溶液生成沉淀的物质的量与NaOH体积关系如图所示,下列离子溶液中能大量共存,加入晶体A后仍能大量共存的是( )| A、Na+、H+、Cl-、NO3- |
| B、K+、Ba2+、OH-、I- |
| C、Mg2+、Fe3+、Br-、HCO3- |
| D、Na+、Mg2+、Cl-、AlO2- |