题目内容
1.对于反应3Cl2+6KOH(浓)═5KCl+KClO3+3H2O,说法正确的是( )| A. | Cl2是氧化剂,KOH是还原剂 | |
| B. | 有3molCl2参加反应,就有6NA个电子转移 | |
| C. | 被还原的氯原子和被氧化的氯原子的个数比是1:1 | |
| D. | 被还原的氯原子和被氧化的氯原子的个数比是5:1 |
分析 反应3Cl2+6KOH=KClO3+5KCl+3H2O中,Cl元素的化合价由0升高为+5价,Cl元素的化合价由0降低为-1价,该反应中转移5e-,以此来解答.
解答 解:A.只有Cl元素的化合价变化,KOH既不是氧化剂,又不是还原剂,故A错误;
B.由化合价变化可知,3mol氯气参加反应转移5mol电子,故B错误;
C.由Cl元素化合价变化可知,生成KCl,Cl元素化合价降低,被还原,生成KClO3,Cl元素化合价升高,被氧化,则被还原的氯原子和被氧化的氯原子的个数比是5:1,故C错误;
D.由反应可知,1molCl被氧化,5molCl被还原,则被还原的氯元素的质量为被氧化的氯元素质量的5倍,被还原的氯原子和被氧化的氯原子的个数比是5:1,故D正确;
故选D.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重基本概念和转移电子数的考查,题目难度不大.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
11.下列变化属于取代反应的是( )
| A. | 苯与溴水混合,水层褪色 | B. | 乙烯使溴的四氯化碳溶液褪色 | ||
| C. | 甲苯制三硝基甲苯 | D. | 苯和氢气在一定条件下生成环已烷 |
12.向10mL0.10mol•L-1某一元酸HA溶液中滴加等浓度的NaOH溶液,滴加过程溶液的pH随滴加NaOH溶液体积的变化如图所示,下列叙述正确的是( )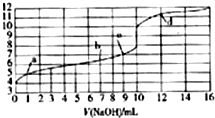

| A. | HA为一元强酸 | |
| B. | 水的电离程度:a点>b点>c点 | |
| C. | c点时,酸和碱恰好完全反应 | |
| D. | d点时,溶液中离子浓度:c(Na+)>c(A-)>c(OH-)>c(H+) |
9. 氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )
 氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )| A. | 该电池中电极b是正极 | |
| B. | 外电路中电子由电极b通过导线流向电极a | |
| C. | 该电池的正极反应为O2+4H++4e-=2H2O | |
| D. | 该电池的总反应:2H2+O2=2H2O |
16.下列说法正确的是( )
| A. | 二氧化硫具有还原性,能与强氧化性的高锰酸钾发生氧化还原反应 | |
| B. | 因为二氧化硫具有漂白性,能使品红溶液永久褪色 | |
| C. | 大气中二氧化碳浓度高时能形成酸雨 | |
| D. | 浓硫酸常用作干燥剂,因为浓硫酸具有脱水性 |
6.市场上有一种加酶洗衣粉,即在洗衣粉中加入少量的碱性蛋白酶,它的催化活性很强,衣物的汗渍、血迹以及人体排放的蛋白质油渍等遇到它,皆能水解而除去.下列衣料中不能用加酶洗衣粉洗涤的是( )
①棉织品 ②毛织品 ③腈纶织品 ④蚕丝织品 ⑤涤纶织品 ⑥尼龙织品.
①棉织品 ②毛织品 ③腈纶织品 ④蚕丝织品 ⑤涤纶织品 ⑥尼龙织品.
| A. | ①②③ | B. | ②④ | C. | ③④⑤ | D. | ③⑤⑥ |
13.符合下列要求的同分异构体数目(不考虑立体异构)最少的是( )
| A. | 分子式为C5H10的烯烃 | B. | 分子式为C5H12O的醇 | ||
| C. | 分子式为C5H10O2的羧酸 | D. | 分子式为C5H10O2的酯 |
10.在25℃时,向10mL0.01mol•L-1NaX溶液中逐滴加入0.01mol•L-1的盐酸溶液,滴定过程中溶液中HX、X-浓度所占分数(φ)随pH的变化曲线如图所示,据此判断下列说法中正确的是( )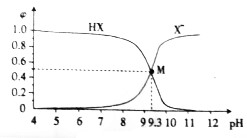

| A. | 25℃时,$\frac{c(HX)}{c({X}^{-})•c({H}^{+})}$=109.3 | |
| B. | M点溶液中存在:c(X-)+c(OH-)=c(H+)+c(Na+) | |
| C. | 滴加盐酸的过程中,水的电离程度先减小后增大 | |
| D. | 常温下,等浓度等体积的HX和NaX溶液混合后,溶液显酸性 |
19.下述实验不能达到预期实验目的是( )
| A. | 向相同体积,相同pH的两种一元酸中分别加入足量锌粉,测量产生氢气的体积,可以比较两种一元酸的酸性相对较弱 | |
| B. | 向盛有1mL硝酸银溶液的试管中滴加NaCl溶液,至恰好不再有沉淀生成,再向其中滴加Na2S溶液,生成黑色沉淀,说明一种沉淀能转化为另一种溶解度更小的沉淀 | |
| C. | 室温下,用pH试纸测定浓度为0.1mol/LNaClO溶液和0.1mol/LCH3COONa溶液的pH,可以比较HClO和CH3COOH的酸性强弱 | |
| D. | 在滴有酚酞Na2CO3溶液中逐滴加入BaCl2溶液,红色逐渐褪去,说明Na2CO3溶液中存在水解平衡 |