题目内容
12.如表实验“操作和现象”与“结论”对应关系正确的是( )| 操作和现象 | 结论 | |
| A | 向氯水中加入硝酸银溶液,有白色沉淀产生 | 氯水中已无Cl2 |
| B | 将SO2通入酸性高锰酸钾溶液,溶液紫色褪去 | SO2具有漂白性 |
| C | 向FeCl3和CuCl2混合溶液中加入少量铁粉,没有红色固体析出 | 氧化性:Fe3+>Cu2+ |
| D | 向某溶液中先滴加硝酸酸化,再滴加BaCl2溶液,有白色沉淀生成 | 该溶液中含有SO42- |
| A. | A | B. | B | C. | C | D. | D |
分析 A、氯气溶于水,部分与水发生反应:Cl2+H2O?HCl+HClO,该反应是可逆反应,所以氯水中含有的微粒是:分子:Cl2、HClO、H2O;离子:H+、Cl-、ClO-、OH-,依据存在微粒的性质解答;
B、将SO2通入酸性高锰酸钾溶液,溶液紫色褪去,说明二氧化硫的还原性;
C、向FeCl3、CuCl2混合溶液加铁粉,先发生Fe与铁离子的反应;
D、能和氯化钡反应生成白色沉淀的离子有硫酸根离子、银离子.
解答 解:A、向氯水中加入硝酸银溶液,有白色沉淀产生,只能说明溶液中存在氯离子,故A错误;
B、将SO2通入酸性高锰酸钾溶液,溶液紫色褪去,说明二氧化硫的还原性,而不是漂白性,故B错误;
C、向FeCl3、CuCl2混合溶液加铁粉,先发生Fe与铁离子的反应生成亚铁离子,再发生Fe与氯化铜反应,则说明氧化性:Cu2+<Fe3+,故C正确;
D、向某溶液中先滴加硝酸酸化,硝酸具有强氧化性,溶液中若是亚硫酸根离子,被硝酸氧化为硫酸根离子,再滴加BaCl2溶液,有白色沉淀生成,溶液中不一定含有银离子,故D错误;
故选C.
点评 本题考查化学实验方案的评价,涉及氯水、还原性、氧化还原反应、离子检验等,侧重反应原理及物质性质的考查,为高频考点,明确物质性质是解本题关键,题目难度不大.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
2.随着原子序数的递增,八种短周期元素(x~h)原子半径的相对大小、最高正价或最低负价的变化如图所示.下列说法错误的是( )

| A. | y在元素周期表的位置是第二周期IVA族 | |
| B. | d元素常见离子的半径大于f元素常见离子的半径 | |
| C. | x,、z元素能组成一种四原子共价化合物,其电子式可以表示为 | |
| D. | e、f的最高价氧化物对应的水化物可以相互反应 |
20.下列说法正确的是( )
| A. | 呈酸性的雨水就是酸雨 | B. | “雷雨肥庄稼”符合科学道理 | ||
| C. | 光化学烟雾是由二氧化硫引起的 | D. | 臭氧层破坏与氮氧化物无关 |
7.鉴别MgSO4、Al2(SO4)3、Fe2(SO4)3、(NH4)2SO4四种溶液,最好选择下列试剂中的( )
| A. | KSCN溶液 | B. | NaOH溶液 | C. | 氨水 | D. | 石蕊试液 |
4.下列元素中一定为主族的是( )
①最高正价为+6价能与氢形成气氢化物
②最外层电子数为1,并且有+1价、+2两种化合价
③除最外层外,其余各电子层都达到了饱和
④最外层电子数是次外层电子数的3倍
⑤最外层电子数为3的一种元素
⑥能形成气态氢化物的一种元素
⑧最高价氧化物对应的水化物是酸的一种元素.
①最高正价为+6价能与氢形成气氢化物
②最外层电子数为1,并且有+1价、+2两种化合价
③除最外层外,其余各电子层都达到了饱和
④最外层电子数是次外层电子数的3倍
⑤最外层电子数为3的一种元素
⑥能形成气态氢化物的一种元素
⑧最高价氧化物对应的水化物是酸的一种元素.
| A. | ①③⑤⑥⑦ | B. | ②④⑥⑦ | C. | ④⑤⑥ | D. | ①③④⑤⑥⑦ |
1.X、Y、Z、W、Q是原子序数依次增大的5种短周期主族元素,X、Z同主族,Y、Q同主族,X是周期表中所有元素原子半径最小的,Y是所有元素中非金属性最强的元素.W元素所处周期的序数等于其族序数.下列说法正确的是( )
| A. | 离子半径:Q>W>Z>Y | |
| B. | 元素Y、Q的气态氢化物稳定性:Q>Y | |
| C. | 元素Z、W、Q的最高价氧化物对应水化物相互间能发生反应 | |
| D. | Y与X、Y与Z形成的化合物化学键类型相同. |
20.下列关于CO2和SO2气体的说法不正确的是( )
| A. | 与足量的澄清石灰水反应的现象不同 | |
| B. | 通入BaCl 2溶液时现象相同 | |
| C. | 通入Ba(NO3)₂溶液时现象相同 | |
| D. | 通入石蕊溶液时现象相同 |
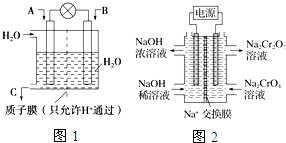 SO2、CO、CO2、NOx是对环境影响较大的几种气体,对它们的合理控制和治理是优化我们生存环境的有效途径.
SO2、CO、CO2、NOx是对环境影响较大的几种气体,对它们的合理控制和治理是优化我们生存环境的有效途径.