题目内容
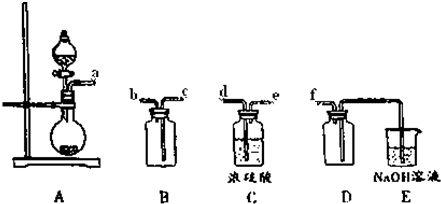
X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族,其中只有两种为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9,单质Y可与NaOH溶液反应生成氢气.下列说法不正确的是( )
| A、原子半径:Y>Z>W |
| B、XW2熔点为107℃,沸点为142.5℃,说明固态XW2为分子晶体 |
| C、电解YW3固体可得单质Y |
D、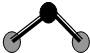 ZW2分子结构见右图,说明ZW2是极性分子 |
考点:原子结构与元素的性质,原子结构与元素周期律的关系
专题:
分析:X、Y、Z、W四种元素的原子序数依次增大,均为短周期元素,且互不同族,X原子的最外层电子数与次外层电子数相等,X只能有2个电子层,最外层电子数为2,则X为Be元素;X与W的最外层电子数之和均为9,则W最外层电子数为7,结合原子序数可知W为Cl,Y与Z这两对原子的最外层电子数之和均为9,结合原子序数可知,最外层电子数为3、6或4、5,且单质Y可与NaOH溶液反应生成氢气,则Y为Al,Z原子最外层电子数为6,故Z为S元素,据此解答.
解答:
解:X、Y、Z、W四种元素的原子序数依次增大,均为短周期元素,且互不同族,X原子的最外层电子数与次外层电子数相等,X只能有2个电子层,最外层电子数为2,则X为Be元素;X与W的最外层电子数之和均为9,则W最外层电子数为7,结合原子序数可知W为Cl,Y与Z这两对原子的最外层电子数之和均为9,结合原子序数可知,最外层电子数为3、6或4、5,且单质Y可与NaOH溶液反应生成氢气,则Y为Al,Z原子最外层电子数为6,故Z为S元素,
A.同周期随原子序数增大,原子半径减小,故原子半径Al>S>Cl,即Y>Z>W,故A正确;
B.BeCl2熔点为107℃,沸点为142.5℃,熔沸点很低,说明固态BeCl2为分子晶体,故B正确;
C.AlCl3属于分子晶体,熔融状态下不能导电,不能电解AlCl3制备Al,工业上通常采取电解熔融氧化铝冶炼Al,故C错误;
D.SCl2分子V形结构,分子中正负电荷重心不重合,SCl2是极性分子,故D正确,
故选C.
A.同周期随原子序数增大,原子半径减小,故原子半径Al>S>Cl,即Y>Z>W,故A正确;
B.BeCl2熔点为107℃,沸点为142.5℃,熔沸点很低,说明固态BeCl2为分子晶体,故B正确;
C.AlCl3属于分子晶体,熔融状态下不能导电,不能电解AlCl3制备Al,工业上通常采取电解熔融氧化铝冶炼Al,故C错误;
D.SCl2分子V形结构,分子中正负电荷重心不重合,SCl2是极性分子,故D正确,
故选C.
点评:本题考查结构性质位置关系应用综合应用,涉及元素周期表、晶体类型与性质、分子结构等,推断元素是解题关键,需要学生具备扎实的基础,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
危险化学药品的包装标签上要印有警示性标志,下列物质选用“易燃品”标志的是( )
| A、酒精 | B、烧碱 |
| C、浓硫酸 | D、氯酸钾 |
未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生.下列属于未来新能源标准的是( )
①太阳能 ②生物质能 ③风能 ④氢能 ⑤煤 ⑥石油 ⑦天然气 ⑧核能.
①太阳能 ②生物质能 ③风能 ④氢能 ⑤煤 ⑥石油 ⑦天然气 ⑧核能.
| A、①②③④ | B、⑤⑥⑦⑧ |
| C、①②③④⑧ | D、①③④⑦⑧ |
氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于区域3的是( )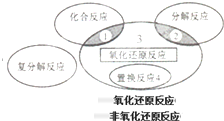

| A、4Fe(OH)2+O2+2H2O=4Fe(OH)3 | ||||
B、2NaHCO3
| ||||
C、4NH3+5O2
| ||||
| D、Zn+H2SO=ZnSO4+H2↑ |
大气中的SO2是造成酸雨的主要污染物,最新研究表明,离子晶体[N(CH3)4]2 SO4(s) 能与SO2进行如下可逆反应,使其可能成为绿色的SO2吸收剂:[N(CH3)4]2 SO4(s)+SO2(g)?[N(CH3)4]2 S2O6(s)下列说法正确的是( )
| A、[N(CH3)4]+中只含共价键 |
| B、该反应中,SO2作氧化剂 |
| C、SO2漂白品红是利用其强氧化性 |
| D、每吸收标准状况下的SO211.2L,生成15.4g[N(CH3)4]2 S2O6 |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、0.5 mol?L-1硫酸钾溶液中阴离子所带电荷数为NA | ||
| B、标准状况下,11.2L氟化氢中含有的氟原子数为0.5NA | ||
C、a g乙烯和环戊烷的混合气中含有极性键数目是
| ||
| D、氢氧燃料电池正极消耗22.4 L(标准状况)气体时,电路中通过的电子数目为2NA |