题目内容
写出下列反应的离子方程式:
(1)二氧化碳通入澄清石灰水变浑浊
(2)Ba(OH)2溶液与硫酸镁溶液反应
(3)NaHSO4溶液与NaHCO3溶液反应
(4)向NaHSO4溶液中,逐渐加入Ba(OH)2溶液至中性,请写出离子方程式: ;
往以上中性溶液中继续滴加Ba(OH)2溶液,请写出此时发生的离子方程式:
(5)向Ba(OH)2溶液中,逐滴加入NaHSO4溶液至恰好不再生成沉淀为止,此时离子方程式为: .
(1)二氧化碳通入澄清石灰水变浑浊
(2)Ba(OH)2溶液与硫酸镁溶液反应
(3)NaHSO4溶液与NaHCO3溶液反应
(4)向NaHSO4溶液中,逐渐加入Ba(OH)2溶液至中性,请写出离子方程式:
往以上中性溶液中继续滴加Ba(OH)2溶液,请写出此时发生的离子方程式:
(5)向Ba(OH)2溶液中,逐滴加入NaHSO4溶液至恰好不再生成沉淀为止,此时离子方程式为:
考点:离子方程式的书写
专题:
分析:(1)二氧化碳少量,氢氧化钙与二氧化碳反应生成碳酸钙和水;
(2)硫酸钡和氢氧化镁都是难溶物,离子方程式中二者都需要保留化学式;
(3)硫酸氢钠完全电离出氢离子,氢离子与碳酸氢根离子反应生成二氧化碳气体和水;
(4)溶液显中性说明硫酸中的氢离子和氢氧化钡中的氢氧根恰好反应,均无剩余,硫酸根离子过量;继续滴加氢氧化钡,硫酸根和钡离子之间反应生成沉淀;
(5)Ba(OH)2溶液中,逐滴加入NaHSO4溶液,硫酸氢钠少量全反应,此时氢氧根应剩余,溶液显示碱性.
(2)硫酸钡和氢氧化镁都是难溶物,离子方程式中二者都需要保留化学式;
(3)硫酸氢钠完全电离出氢离子,氢离子与碳酸氢根离子反应生成二氧化碳气体和水;
(4)溶液显中性说明硫酸中的氢离子和氢氧化钡中的氢氧根恰好反应,均无剩余,硫酸根离子过量;继续滴加氢氧化钡,硫酸根和钡离子之间反应生成沉淀;
(5)Ba(OH)2溶液中,逐滴加入NaHSO4溶液,硫酸氢钠少量全反应,此时氢氧根应剩余,溶液显示碱性.
解答:
解:(1)少量二氧化碳与澄清石灰水反应生成碳酸钙、水,反应的离子反应为:Ca2+20H-+C02=H20+CaC03↓,
故答案为:Ca2+20H-+C02=H20+CaC03↓;
(2)硫酸镁溶液跟氢氧化钡溶液反应生成硫酸钡和氢氧化镁沉淀,反应的离子方程式为:SO42-+Ba2++Mg2++2OH-=Mg(OH)2↓+BaSO4↓,
故答案为:SO42-+Ba2++Mg2++2OH-=Mg(OH)2↓+BaSO4↓;
(3)NaHSO4溶液与NaHCO3溶液反应生成硫酸钠、二氧化碳气体和水,反应的离子方程式为:HCO3-+2H+=CO2↑+H2O,
故答案为:HCO3-+2H+=CO2↑+H2O;
(4)向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至中性,氢氧化钡的量相对于硫酸不足,所以钡离子和氢氧根按照1:2进行反应,即Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,溶液中的硫酸根会和再加入的氢氧化钡中的钡离子反应,即Ba2++SO42-=BaSO4↓,
故答案为:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O;Ba2++SO42-=BaSO4↓;
(5)向Ba(OH)2溶液中,逐滴加入NaHSO4溶液,硫酸氢钠相对于氢氧化钡量少,所以硫酸氢钠全反应,反应的离子方程式为:Ba2++OH-+H++SO42-=BaSO4↓+H2O,所得溶液中氢氧根剩余,
故答案为:Ba2++OH-+H++SO42-=BaSO4↓+H2O.
故答案为:Ca2+20H-+C02=H20+CaC03↓;
(2)硫酸镁溶液跟氢氧化钡溶液反应生成硫酸钡和氢氧化镁沉淀,反应的离子方程式为:SO42-+Ba2++Mg2++2OH-=Mg(OH)2↓+BaSO4↓,
故答案为:SO42-+Ba2++Mg2++2OH-=Mg(OH)2↓+BaSO4↓;
(3)NaHSO4溶液与NaHCO3溶液反应生成硫酸钠、二氧化碳气体和水,反应的离子方程式为:HCO3-+2H+=CO2↑+H2O,
故答案为:HCO3-+2H+=CO2↑+H2O;
(4)向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至中性,氢氧化钡的量相对于硫酸不足,所以钡离子和氢氧根按照1:2进行反应,即Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,溶液中的硫酸根会和再加入的氢氧化钡中的钡离子反应,即Ba2++SO42-=BaSO4↓,
故答案为:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O;Ba2++SO42-=BaSO4↓;
(5)向Ba(OH)2溶液中,逐滴加入NaHSO4溶液,硫酸氢钠相对于氢氧化钡量少,所以硫酸氢钠全反应,反应的离子方程式为:Ba2++OH-+H++SO42-=BaSO4↓+H2O,所得溶液中氢氧根剩余,
故答案为:Ba2++OH-+H++SO42-=BaSO4↓+H2O.
点评:本题考查学生离子方程式的书写,题目难度中等,试题知识点较多,充分考查了学生灵活应用所学知识的能力,注意物质用量的多少所决定的反应产物的情况.

练习册系列答案
相关题目
下列有关物理量相应的单位,表达不正确的是( )
| A、摩尔质量:g?mol-1 |
| B、密度:g?mL-1 |
| C、气体摩尔体积:L |
| D、阿伏加德罗常数:mol-1 |
能正确表示下列化学反应的离子方程式是( )
| A、过量的NaHSO4与Ba(OH)2溶液反应:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
| B、硫酸镁溶液跟氢氧化钡溶液反应:SO42-+Ba2+=BaSO4↓ |
| C、NH4HCO3溶液与过量NaOH溶液反应:NH4++OH-=NH3↑+H2O |
| D、向碳酸氢钠溶液中滴加少量稀硝酸:CO32-+2H +=CO2↑ +H2O |
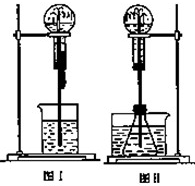
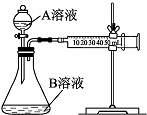 实验小组利用酸性KMnO4溶液与H2C2O4溶液反应研究影响反应速率的因素.
实验小组利用酸性KMnO4溶液与H2C2O4溶液反应研究影响反应速率的因素.
 喷泉是一种常见的实验现象(如图),其产生原因是存在压强差.
喷泉是一种常见的实验现象(如图),其产生原因是存在压强差.