题目内容
在下列各变化中,E为常温下无色无味的液体,F为淡黄色粉末,G为常见的无色气体(反应条件均已省略).
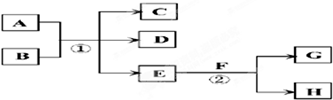
回答下列问题:
(1)写出F的电子式: ;H中所含化学键为 .
(2)若反应①在加热条件下进行,A为单质,C为无色有刺激性气味的气体,D为无色无味的气体,且C、D两种气体均能使澄清的石灰水变浑浊,则反应①的化学方程式是 ,实验需要检验出C、D、E三种气体产物,三种气体检验的先后顺序是 (用化学式填空),在检验D气体前,需除去C气体,所用试剂是 ,反应的离子方程式是 .
(3)若A 与B均为固体化合物,C是常见的一种中性干燥剂,则反应①的化学方程式是 .

回答下列问题:
(1)写出F的电子式:
(2)若反应①在加热条件下进行,A为单质,C为无色有刺激性气味的气体,D为无色无味的气体,且C、D两种气体均能使澄清的石灰水变浑浊,则反应①的化学方程式是
(3)若A 与B均为固体化合物,C是常见的一种中性干燥剂,则反应①的化学方程式是
考点:无机物的推断
专题:
分析:E为常温下无色无味的液体,F为淡黄色粉末,G为常见的无色气体,E为常温下无色无味的液体且在生成物中,所以是水.F为淡黄色粉末,是过氧化钠或硫,但能和水反应,所以是过氧化钠.过氧化钠和水反应的生成物是氧气和氢氧化钠,G为常见的无色气体,所以G是氧气,H是氢氧化钠;
解答:
解:E为常温下无色无味的液体且在生成物中,所以是水.F为淡黄色粉末,是过氧化钠或硫,但能和水反应,所以是过氧化钠.过氧化钠和水反应的生成物是氧气和氢氧化钠,G为常见的无色气体,所以G是氧气,H是氢氧化钠.
(1)F为过氧化钠,电子式为: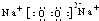 ,H为氢氧化钠,含有离子键和共价键,故答案为:
,H为氢氧化钠,含有离子键和共价键,故答案为: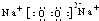 ;离子键、共价键;
;离子键、共价键;
(2)反应①在加热条件下进行,A为单质,C为无色有刺激性气味的气体,D为无色无味的气体,且C、D两种气体均能使澄清的石灰水变浑浊,C、D是二氧化碳和二氧化硫,E为水,所以C、D、E是浓硫酸和碳反应的产物,C、D、E三种气体产物分别为CO2、SO2、H2O;三种气体检验的先后顺序,水蒸气用无水硫酸铜检验,需要放在第一步,二氧化碳和二氧化硫都能和氢氧化钙反应生成沉淀,所以需要第二步检验二氧化硫,除去二氧化硫后再检验二氧化碳气体;除去二氧化硫需要氧化剂为酸性高锰酸钾溶液;发生的反应为酸性溶液中二氧化硫被氧化为硫酸,高锰酸根离子被还原为锰离子,反应的离子方程式为:2MnO4-+5SO2+2H2O=2Mn2++5SO42-+4H+,
故答案为:C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O;H2O、SO2、CO2;酸性高锰酸钾溶液;2MnO4-+5SO2+2H2O=2Mn2++5SO42-+4H+;
(3)若A与B均为固体化合物,C是常见的一种中性干燥剂即氯化钙,所以A和B的反应可以是氯化铵和氢氧化钙生成氨气、氯化钙和水的反应,即2NH4Cl+Ca(OH)2
CaCl2+2H2O+2NH3↑,故答案为:2NH4Cl+Ca(OH)2
CaCl2+2H2O+2NH3↑.
(1)F为过氧化钠,电子式为:
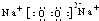 ,H为氢氧化钠,含有离子键和共价键,故答案为:
,H为氢氧化钠,含有离子键和共价键,故答案为: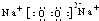 ;离子键、共价键;
;离子键、共价键;(2)反应①在加热条件下进行,A为单质,C为无色有刺激性气味的气体,D为无色无味的气体,且C、D两种气体均能使澄清的石灰水变浑浊,C、D是二氧化碳和二氧化硫,E为水,所以C、D、E是浓硫酸和碳反应的产物,C、D、E三种气体产物分别为CO2、SO2、H2O;三种气体检验的先后顺序,水蒸气用无水硫酸铜检验,需要放在第一步,二氧化碳和二氧化硫都能和氢氧化钙反应生成沉淀,所以需要第二步检验二氧化硫,除去二氧化硫后再检验二氧化碳气体;除去二氧化硫需要氧化剂为酸性高锰酸钾溶液;发生的反应为酸性溶液中二氧化硫被氧化为硫酸,高锰酸根离子被还原为锰离子,反应的离子方程式为:2MnO4-+5SO2+2H2O=2Mn2++5SO42-+4H+,
故答案为:C+2H2SO4(浓)
| ||
(3)若A与B均为固体化合物,C是常见的一种中性干燥剂即氯化钙,所以A和B的反应可以是氯化铵和氢氧化钙生成氨气、氯化钙和水的反应,即2NH4Cl+Ca(OH)2
| ||
| ||
点评:本题考查了物质转化关系的分析判断,物质性质的应用,离子方程式书写方法,熟练掌握物质性质是关键,题目难度中等.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
要使NH4Cl溶液中c(NH4+)=c(Cl-),可向其中加入:( )
| A、NaOH |
| B、盐酸 |
| C、Na2CO3 |
| D、CH3COONH4 |
在①丙烯 ②四氟乙烯 ③氯苯 ④环已烯 四种有机化合物中,分子内所有原子均在同一平面的是( )
| A、①② | B、②④ | C、③④ | D、②③ |
可逆反应A+3B?2C+2D,在不同条件下反应速率最快的是( )
| A、VA=0.5mol/L?s |
| B、VB=0.6mol/L?s |
| C、VC=0.8mol/L?s |
| D、VD=2mol/L?min |
下列关于
He的说法正确的是( )
3 2 |
| A、与 42He互为同位素 |
| B、中子数为3 |
| C、带2个单位正电荷 |
| D、原子最外层有1个电子 |
下列表示正确的是( )
A、N2的电子式: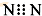 |
B、CS2分子的球棍模型: |
C、邻羟基苯甲酸的结构简式: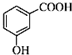 |
D、苯的比例模型: |
下列各式中,属于正确的电离方程式的是( )
| A、HCO3-+H2O?H2CO3+OH- |
| B、CH3COONa?CH3COO-+Na+ |
| C、Ca(OH)2?Ca2++2OH- |
| D、NH3?H2O?NH4++OH- |