题目内容
11.某气态氧化物的化学式为XO2,在标准状况下,1.92g 该氧化物的体积为672mL,则该氧化物的摩尔质量为64g/mol.分析 根据n=$\frac{V}{{V}_{m}}$计算该氧化物的物质的量,根据M=$\frac{m}{n}$计算其摩尔质量,由此分析解答.
解答 解:标况下,1.92g该氧化物的体积为672mL,其物质的量为$\frac{0.672L}{22.4L/mol}$=0.03mol,故该氧化物的摩尔质量=$\frac{1.92g}{0.03mol}$=64g/mol,
故答案为:64g/mol.
点评 本题考查物质的量的相关计算,需要学生熟练掌握基础知识,有利于学生基础知识的巩固,难度不大.

练习册系列答案
相关题目
1.下列有关物质分类正确的是( )
| 选项 | 类别 | 物质 |
| A | 碱性氧化物 | Na2O2 Al2O3 MgO |
| B | 酸式盐 | NaHCO3 NaHSO4 NH4Cl |
| C | 弱酸 | H2S H2SO4 CH3COOH |
| D | 强电解质 | AgCl MgSO4 CaCO3 |
| A. | A | B. | B | C. | C | D. | D |
2.下列有关表达不正确的是( )
| A. | 符号为${\;}_8^{18}$O的原子常用于文物年代的测定 | |
| B. | 原子结构示意图 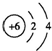 既可以表示12C,也可以表示14C 既可以表示12C,也可以表示14C | |
| C. | 具有16个质子、16个中子和18个电子的微粒是${\;}_{16}^{32}$S2- | |
| D. | “84消毒液”中有效成分NaClO的电子式为  |
19.有机化合物M的结构简式为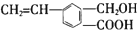 ,关于M的说法正确的是( )
,关于M的说法正确的是( )
 ,关于M的说法正确的是( )
,关于M的说法正确的是( )| A. | 分子式为C10H12O3 | |
| B. | 1 molNa2CO3,最多能消耗l mol有机物M | |
| C. | 1 molM与足量金属钠反应生成11.2 L气体(标准状况) | |
| D. | M能发生取代反应、氧化反应和加成反应 |
6.除去下列括号内杂质的试剂或方法错误的是( )
| A. | HNO3溶液(H2SO4),适量BaCl2溶液,过滤 | |
| B. | CO2(SO2),酸性KMnO4溶液、浓硫酸,洗气 | |
| C. | FeCl2溶液(FeCl3),铁粉,过滤 | |
| D. | CO(CO2),氢氧化钠溶液,洗气 |

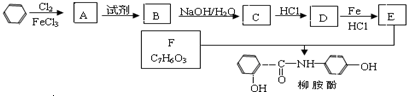
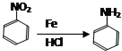
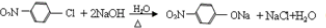 .
.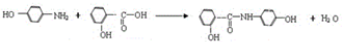 .
. .
.