题目内容
将固体NH4I置于密闭容器中,在一定温度下发生下列反应:
①NH4I(s) NH3(g)+HI(g);②2HI(g)
NH3(g)+HI(g);②2HI(g) H2(g)+I2(g)。达到平衡时,c(H2)=0.5 mol/L,c(HI)=4 mol/L,则此温度下反应①的平衡常数为
H2(g)+I2(g)。达到平衡时,c(H2)=0.5 mol/L,c(HI)=4 mol/L,则此温度下反应①的平衡常数为
①NH4I(s)
 NH3(g)+HI(g);②2HI(g)
NH3(g)+HI(g);②2HI(g) H2(g)+I2(g)。达到平衡时,c(H2)=0.5 mol/L,c(HI)=4 mol/L,则此温度下反应①的平衡常数为
H2(g)+I2(g)。达到平衡时,c(H2)=0.5 mol/L,c(HI)=4 mol/L,则此温度下反应①的平衡常数为[ ]
A.9
B.16
C.20
D.25
B.16
C.20
D.25
C

练习册系列答案
 巧学巧练系列答案
巧学巧练系列答案
相关题目
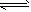 CO(g)+3H2(g);△H= +206.1 kJ/mol
CO(g)+3H2(g);△H= +206.1 kJ/mol 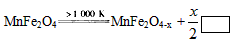 则框内的物质为:________; 第二步反应方程式为:
则框内的物质为:________; 第二步反应方程式为: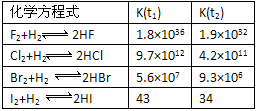
 ,在2min时反应达到平衡状态,此时容器中剩余0.6mol B,并测得C的浓度为0.6 mol·L-1。计算:
,在2min时反应达到平衡状态,此时容器中剩余0.6mol B,并测得C的浓度为0.6 mol·L-1。计算: CO(g)+H2(g),其平衡常数表达式正确的是
CO(g)+H2(g),其平衡常数表达式正确的是 
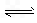 H2S(g) K1
H2S(g) K1  SO2(g) K2
SO2(g) K2  O2+H2S的平衡常数为
O2+H2S的平衡常数为