题目内容
某短周期元素X,其原子的电子层数为n,最外层电子数为(2n+1),原子核内质子数是(2n2-1).下列有关X的说法,不正确的是( )
| A、X是非金属元素 |
| B、X可能形成化学式为KXO3的含氧酸钾盐 |
| C、由X形成的含氧酸均为强酸 |
| D、X不可能为第一周期元素 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:短周期元素X,其原子的电子层数为n,最外层电子数为2n+1,原子核内质子数是2n2-1,若n=1时,最外层电子数为3,不符合题意;n=2时,最外层电子数为5,质子数为7,符合题意;n=3时,最外层电子数为7,质子数为17,符合题意,以此来解答.
解答:
解:短周期元素X,其原子的电子层数为n,最外层电子数为2n+1,原子核内质子数是2n2-1,若n=1时,最外层电子数为3,不符合题意;n=2时,最外层电子数为5,质子数为7,符合题意;n=3时,最外层电子数为7,质子数为17,符合题意,
A.X元素为N或Cl,都是属于非金属元素,故A正确;
B.X元素为N或Cl,可形成KNO3或KClO3,故B正确;
C.氯元素形成的HClO为弱酸,故C错误;
D.X元素为N或Cl,处于第二或第三周期,故D正确,
故选C.
A.X元素为N或Cl,都是属于非金属元素,故A正确;
B.X元素为N或Cl,可形成KNO3或KClO3,故B正确;
C.氯元素形成的HClO为弱酸,故C错误;
D.X元素为N或Cl,处于第二或第三周期,故D正确,
故选C.
点评:本题考查原子结构与元素周期律关系,注意利用讨论法解答,难度不大.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
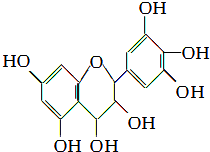 从葡萄籽中提取的原花青素结构为:原花青素具有生物活性,如抗氧化和自由基清除能力等,可防止机体内脂质氧化和自由基的产生而引发的肿瘤等多种疾病.有关原花青素的下列说法不正确的是( )
从葡萄籽中提取的原花青素结构为:原花青素具有生物活性,如抗氧化和自由基清除能力等,可防止机体内脂质氧化和自由基的产生而引发的肿瘤等多种疾病.有关原花青素的下列说法不正确的是( )| A、该物质既可看作醇类,也可看作酚类 |
| B、1 mol该物质可与4 mol Br2反应 |
| C、1 mol该物质可与7 mol NaOH反应 |
| D、1 mol该物质可与7 mol Na反应 |
新产品“不粘锅”受到广大群众的欢迎,其生产工艺十分简单:在金属锅的内壁上涂一层聚四氟乙烯.下列说法中正确的是( )
| A、聚四氟乙烯的结构简式是:F2C=CF2 |
| B、聚四氟乙烯中含碳,所以在加热时能够燃烧生成二氧化碳 |
| C、由于C-C键和F-C键很牢固,因而聚四氟乙烯的性质稳定,在使用时不会污染食物 |
| D、聚四氟乙烯中不能与常见的氧化剂接触,防止被氧化 |
下列说法正确的是( )
| A、甲烷和乙烯都可以与氯气反应 |
| B、乙炔可以与氢气发生加成反应,苯不能与氢气加成 |
| C、除去乙烷中少量的乙烯:光照条件下通入Cl2,气液分离 |
| D、高锰酸钾可以氧化苯和甲烷 |
已知25℃时有关物质的电离平衡常数:
下列叙述错误的是( )
| 弱酸 | CH3COOH | 苯酚 | H2CO3 |
| 电离平衡常数 | 1.75×l0-5 | 1.1×l0-10 | K1=4.4×l0-7 K2=4.7×l0-11 |
| A、等物质的量浓度的各溶液pH关系为:pH(C6H5ONa)>pH(Na2CO3)>pH(NaHCO3)>pH(CH3COONa) |
| B、向苯酚钠溶液中通入少量CO2气体反应为:C6H5O-+H2O+CO2→C6H5OH+HCO3- |
| C、等物质的量浓度的苯酚稀溶液与NaOH稀溶液等体积混合后溶液中:c(Na+)>c(C6H5O-)>c(OH-)>c(H+) |
| D、NaHCO3和Na2CO3混合液中,一定有c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) |
下列化学反应的离子方程式书写正确的是( )
| A、氯化铝溶液与过量氨水反应:3OH-+Al3+═Al(OH)3↓ |
| B、铜溶于稀硝酸:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O |
| C、FeCl3溶液与Cu粉反应:Cu+Fe3+═Cu2++Fe2+ |
| D、次氯酸钙溶液中通入过量CO2:Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO |
下列有关说法正确的是( )
| A、CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△H>0 |
| B、放热反应的反应速率总是大于吸热反应的反应速率 |
| C、N2(g)+3H2(g)?2NH3(g)△H<0,其他条件不变时升高温度,反应速率V(H2)和氢气的平衡转化率均增大 |
| D、液氨是一种重要的制冷剂,说明氨气在液化时吸收大量的热 |
下列叙述中不正确的是( )
| A、同分异构体的化学性质不一定相同 |
| B、同素异形体的化学性质不一定相同 |
| C、同位素原子的化学性质不一定相同 |
| D、同系物的物质物理性质不一定相同 |
下列叙述正确的是( )
| A、将5.85gNaCl晶体溶入100mL水中,制得1mol/L的NaCl溶液 |
| B、11.2LHCl气体溶于水配成0.5L溶液,其浓度为1mol/L |
| C、浓度为2.00 mol/L的盐酸溶液1L,将溶液加热蒸发浓缩至0.5L 其浓度小于4.00mol/L |
| D、向100mL1mol/LCuSO4溶液加入25g 胆矾晶体,溶液浓度变为2mol/L |