题目内容
19.按要求写出反应方程式①H++OH-=H2O(写出对应的化学方程式)HCl+NaOH=NaCl+H2O
②CaCO3+2H+═Ca2++CO2↑+H2O(写出对应的化学方程式)CaCO3+2HCl═CaCl2+CO2↑+H2O
③向澄清石灰水中通入过量CO2(写出对应离子方程式)CO2+OH-=HCO3-
④向NaHSO4溶液中滴入Ba(OH)2溶液至SO42-恰好完全沉淀(写出对应离子方程式)H++SO42-+Ba2++OH-=BaSO4↓+H2O
(已知NaHSO4=Na++H++SO42-)
分析 ①H++OH-=H2O表示强酸或者可溶性强酸的酸式盐和可溶性强碱;
②CaCO3+2H+═Ca2++CO2↑+H2O表示碳酸钙和可溶性强酸反应生成可溶性 盐和二氧化碳、水;
③向澄清石灰水中通入过量CO2,反应生成碳酸氢钙;
④原溶液中的SO42-恰好完全沉淀,则硫酸氢钠和氢氧化钡应该以1:1反应,二者反应生成硫酸钡、氢氧化钠和水.
解答 解:①H++OH-=H2O表示强酸或者可溶性强酸的酸式盐和可溶性强碱,可表示盐酸与氢氧化钠反应,化学方程式:HCl+NaOH=NaCl+H2O;
故答案为:HCl+NaOH=NaCl+H2O;
②CaCO3+2H+═Ca2++CO2↑+H2O表示碳酸钙和可溶性强酸反应生成可溶性 盐和二氧化碳、水,可表示碳酸钙与盐酸反应,化学方程式:CaCO3+2HCl═CaCl2+CO2↑+H2O;
③向澄清石灰水中通入过量CO2,反应生成碳酸氢钙,离子方程式:CO2+OH-=HCO3-;
故答案为:CO2+OH-=HCO3-;
④原溶液中的SO42-恰好完全沉淀,则硫酸氢钠和氢氧化钡应该以1:1反应,二者反应生成硫酸钡、氢氧化钠和水,离子方程式为H++SO42-+OH-+Ba2+=BaSO4+H2O,
故答案为:H++SO42-+OH-+Ba2+=BaSO4+H2O;
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意化学式的拆分,注意反应物用量对反应的影响,题目难度不大.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
9.某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①碱式滴定管用蒸馏水洗净后,用待测溶液润洗2~3次后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中;
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;
③向锥形瓶中滴入酚酞作指示剂,进行滴定.滴定至指示剂恰好变色,且半分钟不变化,测得所耗盐酸的体积为V1mL;
④重复以上过程,但滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL.
(1)滴定终点时的现象为锥形瓶中的溶液由粉红色变为无色且在半分钟内不恢复
(2)该小组在步骤①中的错误是_待测溶液润洗锥形瓶,由此造成的测定结果偏高;(填偏高、偏低或无影响);
(3)步骤②缺少的操作是用标准液润洗滴定管2~3次;
(4)根据下列数据:
计算待测烧碱溶液的浓度为0.0800 mol/L.
①碱式滴定管用蒸馏水洗净后,用待测溶液润洗2~3次后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中;
②将酸式滴定管用蒸馏水洗净后,立即向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;
③向锥形瓶中滴入酚酞作指示剂,进行滴定.滴定至指示剂恰好变色,且半分钟不变化,测得所耗盐酸的体积为V1mL;
④重复以上过程,但滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL.
(1)滴定终点时的现象为锥形瓶中的溶液由粉红色变为无色且在半分钟内不恢复
(2)该小组在步骤①中的错误是_待测溶液润洗锥形瓶,由此造成的测定结果偏高;(填偏高、偏低或无影响);
(3)步骤②缺少的操作是用标准液润洗滴定管2~3次;
(4)根据下列数据:
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 25.00 | 0.40 | 20.38 |
| 第二次 | 25.00 | 4.00 | 24.02 |
10. 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
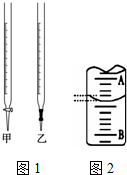
①取一支图1所示仪器,用蒸馏水洗净,即加入待测的NaOH溶液,
使尖嘴部分充满溶液,并调整液面处于“0“刻度以下的位置,记下读数;
②取锥形瓶用蒸馏水洗净,精确量取一定量的0.1000mol•L-1标准盐酸;
③加入3滴酚酞试液,摇匀;
④进行滴定实验,并记录数据.
⑤重复以上步骤2次.
回答下列问题:
(1)步骤①中应将NaOH溶液注入图中的碱式滴定管(填仪器名称)中.
(2)在步骤①中存在的明显错误是滴定管没有用待测NaOH溶液润洗,由此会使测定结果偏低(选填“偏高”、“偏低”或“无影响”).
(3)图2是某次实验中液面位置示意图,若A与B刻度间相差1mL,A处的刻度为19,滴定管中液面读数应为19.40mL.
(4)操作④中左手轻轻挤压玻璃球,右手振荡锥形瓶,眼睛注视锥形瓶内溶液颜色的变化,能确定实验终点的现象是加入最后一滴液体,溶液由无色变成浅红色,且半分钟内不褪色.
(5)根据下列数据:
计算待测烧碱溶液的浓度为0.1053 mol/L(保留至小数点后四位).
 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:①取一支图1所示仪器,用蒸馏水洗净,即加入待测的NaOH溶液,
使尖嘴部分充满溶液,并调整液面处于“0“刻度以下的位置,记下读数;
②取锥形瓶用蒸馏水洗净,精确量取一定量的0.1000mol•L-1标准盐酸;
③加入3滴酚酞试液,摇匀;
④进行滴定实验,并记录数据.
⑤重复以上步骤2次.
回答下列问题:
(1)步骤①中应将NaOH溶液注入图中的碱式滴定管(填仪器名称)中.
(2)在步骤①中存在的明显错误是滴定管没有用待测NaOH溶液润洗,由此会使测定结果偏低(选填“偏高”、“偏低”或“无影响”).
(3)图2是某次实验中液面位置示意图,若A与B刻度间相差1mL,A处的刻度为19,滴定管中液面读数应为19.40mL.
(4)操作④中左手轻轻挤压玻璃球,右手振荡锥形瓶,眼睛注视锥形瓶内溶液颜色的变化,能确定实验终点的现象是加入最后一滴液体,溶液由无色变成浅红色,且半分钟内不褪色.
(5)根据下列数据:
| 滴定次数 | 标准盐酸体积/mL | 待测液体积/mL | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.52 | 19.42 |
| 第二次 | 20.00 | 4.07 | 23.17 |
| 第三次 | 20.00 | 1.08 | 20.08 |
8.下列溶液中Cl-的物质的量浓度最大的是( )
| A. | 10 mL 0.1 mol/L AlCl3溶液 | B. | 20 mL 0.1 mol/L CaCl2溶液 | ||
| C. | 30 mL 0.2 mol/L KCl溶液 | D. | 200 mL 2 mol•L-1KClO3溶液 |
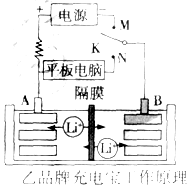 充电宝基本都由聚合物锂电池作为储电单元,它本身就是一个聚合物锂电池的储电装置,通过IC芯片进行电压的调控,再通过连接电源线充电或储电后将贮存的电量释放出来.
充电宝基本都由聚合物锂电池作为储电单元,它本身就是一个聚合物锂电池的储电装置,通过IC芯片进行电压的调控,再通过连接电源线充电或储电后将贮存的电量释放出来.