题目内容
室温下,将1mol的CuSO4·5H2O(s)溶于水会使溶液温度降低,热效应为ΔH1,将1mol的CuSO4(s)溶于水会使溶液温度升高,热效应为ΔH2;CuSO4·5H2O受热分解的化学方程式为:CuSO4·5H2O(s)
 CuSO4 (s) +5H2O(l),热效应为ΔH3。则下列判断正确的是
CuSO4 (s) +5H2O(l),热效应为ΔH3。则下列判断正确的是
A.ΔH2>ΔH3 B.ΔH1<ΔH3 C.ΔH1+ΔH3=ΔH2 D.ΔH1+ΔH2=ΔH3
B
【解析】
试题分析:根据题意结合盖斯定律可得ΔH2+ΔH3=ΔH1;1mol的CuSO4·5H2O(s)溶于水会使溶液温度降低,热效应为ΔH1>0,将1mol的CuSO4(s)溶于水会使溶液温度升高,热效应为ΔH2<0;CuSO4·5H2O受热分解的化学方程式为:CuSO4·5H2O(s) 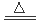 CuSO4 (s) +5H2O(l),热效应为ΔH3>0。所以ΔH3>ΔH1.因此选项是B。
CuSO4 (s) +5H2O(l),热效应为ΔH3>0。所以ΔH3>ΔH1.因此选项是B。
考点:考查盖斯定律的应用的知识。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
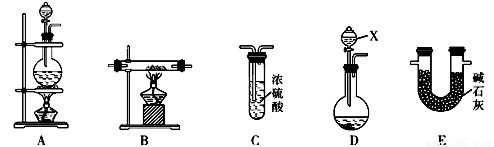
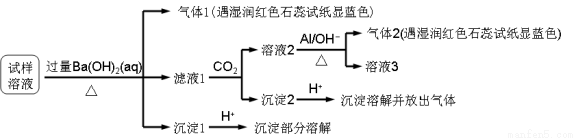
 3NH3 + 8AlO2-
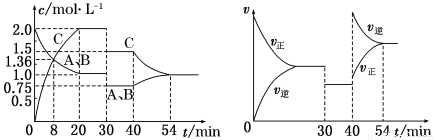
3NH3 + 8AlO2- 2C(g),达到平衡后,在不同的时间段,下列说法中正确的是
2C(g),达到平衡后,在不同的时间段,下列说法中正确的是